Để sản xuất nhôm cần phải có một nguồn điện năng dồi dào. Vậy quy trình luyện nhôm đã dựa trên hiện tượng nào để đòi hỏi cần nhiều điện như vậy?
Sau khi học xong bài mới- Bài 14: Dòng điện trong chất điện phân các em sẽ trả lời được câu hỏi trên. Mời các em cùng theo dõi nội dung bài học nhé.
Trong dung dịch, các hợp chất hoá học như axit, bazơ và muối bị phân li thành các nguyên tử tích điện gọi là ion; ion có thể chuyển động tự do trong dung dịch và trở thành hạt tải điện.
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của các ion trong điện trường.
Chất điện phân không dẫn điện tốt bằng kim loại.
Dòng điện trong chất điện phân không chỉ tải điện lượng mà còn tải cả vật chất đi theo. Tới điện cực chỉ có các electron có thể đi tiếp, còn lượng vật chất đọng lại ở điện cực, gây ra hiện tượng điện phân
Ion dương (Cation) -> Catot
Ion âm (Anion) -> Anot
Các ion chuyển động về các điện cực có thể tác dụng với chất làm điện cực hoặc với dung môi tạo nên các phản ứng hoá học gọi là phản ứng phụ trong hiện tượng điện phân.
Hiện tượng dương cực tan xảy ra khi các anion đi tới anôt kéo các ion kim loại của điện cực vào trong dung dịch
Khối lượng vật chất được giải phóng ở điện cực của bình điện phân tỉ lệ thuận với điện lượng chạy qua bình đó.
\(m = k.q\)
k: đương lượng điện hóa của chất được giải phóng
Đương lượng điện hoá k của một nguyên tố tỉ lệ với đương lượng gam \(\frac{A}{n}\) của nguyên tố đó. Hệ số tỉ lệ \(\frac{1}{F}\) , trong đó F gọi là số Faraday.
\(k = \frac{1}{F}.\frac{A}{n}\)
F = 96500 C/mol
A: khối lượng phân tử
n: hóa trị
Kết hợp hai định luật Fa-ra-đây, ta được công thức Fa-ra-đây
\(m = \frac{1}{F}.\frac{A}{n}.I.t\)
m: khối lượng chất được giải phóng (g)
F = 96500 C/mol
A: khối lượng phân tử
n: hóa trị
I: cường độ dòng điện
t: thời gian dòng điện chạy qua.
Hiện tượng điện phân có nhiều ứng dụng trong thực tế sản xuất và đời sống như luyện nhôm, tinh luyện đồng, điều chế clo, xút, mạ điện, đúc điện, …
Dựa vào hiện tượng điện phân quặng nhôm nóng chảy.
Bể điện phân có cực dương là quặng nhôm nóng chảy, cực âm bằng than, chất điện phân là muối nhôm nóng chảy, dòng điện chạy qua khoảng \({10^4}A\)
Bể điện phân có anôt là một tấm kim loại để mạ, catôt là vật cần mạ.
Chất điện phân thường là dung dịch muối kim loại để mạ. Dòng điện qua bể mạ được chọn một cách thích hợp để đảm bảo chất lượng của lớp mạ.
Phát biểu nào sau đây chính xác
Kết quả cuối cùng của quá trình điện phân dung dịch CuSO4 với điện cực bằng đồng là
A. Không có thay đổi gì ở bình điện phân
B. Anôt bị ăn mòn
C. Đồng bám vào catôt
D. Đồng chạy từ anôt sang catôt
Kết quả cuối cùng của quá trình điện phân dung dịch CuSO4 với điện cực bằng đồng là đồng chạy từ anôt sang catôt.
⇒ Đáp án D
Phát biểu nào là chính xác
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của
A. Các chất tan trong dung dịch
B. Các ion dương trong dung dịch
C. Các ion dương và ion âm dưới tác dụng của điện trường trong dung dịch
D. Các ion dương và ion âm theo chiều điện trường trong dung dịch
Các ion dương và ion âm dưới tác dụng của điện trwòng trong dung dịch
⇒ Đáp án C.
Tốc độ chuyển động có hướng của ion \(Na^+\) và \(Cl^-\) trong nước có thể tính theo công thức:\(v = \mu E\), trong đó E là cường độ điện trường, \(\mu\) có giá trị lần lượt là \(4,5.10^{-8} m^2/(V.s)\). Tính điện trở suất của dung dịch NaCl nồng độ 0,1 mol/l, cho rằng toàn bộ các phân tử NaCl đều phân li thành ion.
Mật độ của các ion \(Na^+\) và \(Cl^-\):
\(N = 0,1.1000.6,023.10^{23} = 6,023.10^{25}/m^3\)
Điện dẫn suất của dung dịch:
\(\sigma = 1,{6.10^{ - 19}}.6,{023.10^{25}}.(4,5 + 6,8){.10^{ - 8}} = 1,088{(\Omega /m)^{ - 1}}\)
⇒ Điện trở suất \(\rho =\frac{1}{\sigma }=\frac{1}{1,088}=0,92\Omega .m\)
Người ta muốn bóc một lớp đồng dày \(d = 10 \mu m\) trên một bản đồng diện tích \(S = 1cm^2\) bằng phương pháp điện phân. Cường độ dòng điện là 0,010A. Tính thời gian cần thiết để bóc được lớp đồng. Cho biết đồng có khối lượng riêng là \(p = 8 900 kg/m^3\)
Khối lượng đồng phải bóc đi là: \(m = 8 900.1.10^{-4}.10.10^{-6} = 8,9.10^{-6} kg\)
Theo công thức Fa-ra-đây: \(m = \frac{1}{F}.\frac{A}{n}It\) ⇔ m = 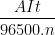 ; suy ra t =
; suy ra t = 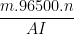
Với \(A = 64g = 6,{4.10^{ - 2}}kg;{\rm{ }}n{\rm{ }} = 2;{\rm{ }}I{\rm{ }} = {10^{ - 2}}A\) , suy ra:
t = 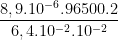 = 2 683,9 s
= 2 683,9 s
Để tách đồng ra khỏi một hỗn hợp rắn chứa 12% tạp chất khác người ta dùng thanh hỗn hợp này làm cực dương của bình điện phân đựng dung dịch \(CuS{O_4}.\) Hiệu điện thế giữa hai cực là \(U = 6(V)\). Tính điện năng tiêu hao để xử lý \(1 (kg)\) hỗn hợp ?
Khối lượng đồng có trong thanh :
\({m_{Cu}} = \frac{{(100 - 12)}}{{100}}m = 0,88(kg)\)
Theo công thức Định luật Faraday :
\(\begin{array}{l}
m = \frac{1}{F}.\frac{A}{n}q\\
\Leftrightarrow 880 = \frac{1}{{96500}}.\frac{{64}}{2}q \Rightarrow q = {2654.10^3}(C)
\end{array}\)
Điện năng tiêu hao để xử lý \(1 (kg)\) hỗn hợp :
\(W = qU = {2654.10^3}.6 = 15923{\rm{ }}\left( {kJ} \right) = 4,42\left( {kWh} \right)\)
Qua bài giảng Dòng điện trong chất điện phân này, các em cần hoàn thành 1 số mục tiêu mà bài đưa ra như :
Trả lời được câu hỏi thế nào là chất điện phân, hiện tượng điện phân, nêu được bản chất dòng điện trong chất điện phân
Phát biểu được định luật Fa-ra-day về điện phân.
Mô tả được hiện tượng dương cực tan
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Vật lý 11 Bài 14 cực hay có đáp án và lời giải chi tiết.
Muốn mạ đồng một tấm sắt có diện tích tổng cộng 200 cm2 , người ta dùng tấm sắt làm catôt của một bình điện phân đựng dùng dịch CuSO4 và anôt là một thanh đồng nguyên chất, rồi cho dòng điện có cường độ \(I = 10A\) chạy qua trong thời gian 2 giờ 40 phút 50 giây. Tìm bề dày lớp đồng bám trên mặt tấm sắt. Cho biết đồng có \(A = 64; n = 2\) và có khối lượng riêng \(\rho = 8,9.103{\rm{ }}kg/{m^3}\)
Chiều dày của một lớp niken phủ lên một tấm kim loại là \(h =0,05mm\) sau khi điện phân trong 30 phút. Diện tích mặt phủ của tấm kim loại là 30 cm2. Xác định cường độ dòng điện chạy qua bình điện phân. Biết niken có \( A = 58,n = 2\) và có khối lượng riêng là \(\rho = 8,9{\rm{ }}g/c{m^3}.\)
Một bộ nguồn điện gồm 30 pin mắc thành 3 nhóm nối tiếp, mỗi nhóm có 10 pin mắc song song; mỗi pin có suất điện động 0,9 V và điện trở trong \(0,6\Omega \). Một bình điện phân đựng dung dịch CuSO4 có điện trở \(205\Omega \) được mắc vào hai cực của bộ nguồn nói trên. Anôt của bình điện phân bằng đồng. Tính khối lượng đồng bám vào catôt của bình trong thời gian 50 phút. Biết Cu có \( A = 64; n = 2.\)
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Vật lý 11 Bài 14để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Bài tập 1 trang 85 SGK Vật lý 11
Bài tập 2 trang 85 SGK Vật lý 11
Bài tập 3 trang 85 SGK Vật lý 11
Bài tập 4 trang 85 SGK Vật lý 11
Bài tập 5 trang 85 SGK Vật lý 11
Bài tập 6 trang 85 SGK Vật lý 11
Bài tập 7 trang 85 SGK Vật lý 11
Bài tập 8 trang 85 SGK Vật lý 11
Bài tập 9 trang 85 SGK Vật lý 11
Bài tập 10 trang 85 SGK Vật lý 11
Bài tập 11 trang 85 SGK Vật lý 11
Bài tập 1 trang 100 SGK Vật lý 11 nâng cao
Bài tập 2 trang 100 SGK Vật lý 11 nâng cao
Bài tập 3 trang 100 SGK Vật lý 11 nâng cao
Bài tập 14.1 trang 35 SBT Vật lý 11
Bài tập 14.2 trang 35 SBT Vật lý 11
Bài tập 14.3 trang 36 SBT Vật lý 11
Bài tập 14.4 trang 36 SBT Vật lý 11
Bài tập 14.5 trang 36 SBT Vật lý 11
Bài tập 14.6 trang 36 SBT Vật lý 11
Bài tập 14.7 trang 37 SBT Vật lý 11
Bài tập 14.8 trang 37 SBT Vật lý 11
Bài tập 14.9 trang 37 SBT Vật lý 11
Bài tập 14.10* trang 37 SBT Vật lý 11
Bài tập 14.11 trang 37 SBT Vật lý 11
Bài tập 14.12* trang 37 SBT Vật lý 11
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Vật lý DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
-- Mod Vật Lý 11 DapAnHay
Muốn mạ đồng một tấm sắt có diện tích tổng cộng 200 cm2 , người ta dùng tấm sắt làm catôt của một bình điện phân đựng dùng dịch CuSO4 và anôt là một thanh đồng nguyên chất, rồi cho dòng điện có cường độ \(I = 10A\) chạy qua trong thời gian 2 giờ 40 phút 50 giây. Tìm bề dày lớp đồng bám trên mặt tấm sắt. Cho biết đồng có \(A = 64; n = 2\) và có khối lượng riêng \(\rho = 8,9.103{\rm{ }}kg/{m^3}\)
Chiều dày của một lớp niken phủ lên một tấm kim loại là \(h =0,05mm\) sau khi điện phân trong 30 phút. Diện tích mặt phủ của tấm kim loại là 30 cm2. Xác định cường độ dòng điện chạy qua bình điện phân. Biết niken có \( A = 58,n = 2\) và có khối lượng riêng là \(\rho = 8,9{\rm{ }}g/c{m^3}.\)
Một bộ nguồn điện gồm 30 pin mắc thành 3 nhóm nối tiếp, mỗi nhóm có 10 pin mắc song song; mỗi pin có suất điện động 0,9 V và điện trở trong \(0,6\Omega \). Một bình điện phân đựng dung dịch CuSO4 có điện trở \(205\Omega \) được mắc vào hai cực của bộ nguồn nói trên. Anôt của bình điện phân bằng đồng. Tính khối lượng đồng bám vào catôt của bình trong thời gian 50 phút. Biết Cu có \( A = 64; n = 2.\)
Hai bình điện phân: (CuSO4/Cu và AgNO3/Ag) mắc nối tiếp. Trong một mạch điện. Sau một thời gian điện phân, khối lượng catôt của hai bình tăng lên 2,8 g. Biết nguyên tử lượng của đồng và bạc là 64 và 108, hóa trị của đồng và bạc là 2 và 1. Tính khối lượng Ag được giải phóng ở catôt
Hai bình điện phân: \((FeC{l_3}/Fe\) và CuSO4/Cu) mắc nối tiếp. Sau một khoảng thời gian, bình thứ nhất giải phóng một lượng sắt là 1,4 g. Tính lượng đồng giải phóng ở bình thứ hai trong cùng khoảng thời gian đó. Biết nguyên tử lượng của đồng và sắt là 64 và 56, hóa trị của đồng và sắt là 2 và 3.
Một bình điện phân đựng dung dịch bạc Nitrat với Anốt làm bằng bạc. Điện trở của bình điện phân là \(R = 2\Omega \) . Hiệu điện thế đặt ở hai cực là \(U = 10(V)\). Cho \(A = 108, n = 1\). Khối lượng bạc bám vào cực âm sau 2 giờ là
Kết quả cuối cùng của quá trình điện phân dung dịch CuSO4 với điện cực bằng đồng là
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của
Tốc độ chuyển động có hướng của ion \(Na^+\) và \(Cl^-\) trong nước có thể tính theo công thức:\(v = \mu E\), trong đó E là cường độ điện trường, \(\mu\) có giá trị lần lượt là \(4,5.10^{-8} m^2/(V.s)\). Tính điện trở suất của dung dịch NaCl nồng độ 0,1 mol/l, cho rằng toàn bộ các phân tử NaCl đều phân li thành ion.
Để tách đồng ra khỏi một hỗn hợp rắn chứa 12% tạp chất khác người ta dùng thanh hỗn hợp này làm cực dương của bình điện phân đựng dung dịch \(CuS{O_4}.\) .Hiệu điện thế giữa hai cực là \(U = 6(V)\). Tính điện năng tiêu hao để xử lý \(1 (kg)\) hỗn hợp ?
Nội dung của thuyết điện li là gì? Anion thường là phần nào của phân tử?
Dòng điện trong chất điện phân khác với dòng điện trong kim loại như thế nào?
Hãy nói rõ hạt tải điện nào mang dòng điện trên các phần khác nhau của mạch điện có chứa bình điện phân:
a. Dây dẫn và điện cực
b. Ở sát bề mặt hai điện cực
c. Ở trong lòng chất điện phân: ở trong lòng chất điện phân, hạt tải điện là
Chất điện phân thường dẫn điện tốt hơn hay kém hơn kim loại? Tại sao?
Hai bể điện phân: bể A để luyện nhôm, bể B để mạ niken. Hỏi bể nào có dương cực tan? Bể nào có suất phản điện?
Phát biểu định luật Pha-ra-đây, viết công thức Fa-ra-đây và đơn vị dùng trong công thức này.
Khi điện phân dung dịch \(H_2SO_4\) với điện cực bằng graphit, thì ta thu được khí oxi bay ra. Có thể dùng công thức Fa-ra-đây để tìm khối lượng oxi bay ra được không?
Phát biểu nào là chính xác
Dòng điện trong chất điện phân là dòng chuyển dời có hướng của
A. Các chất tan trong dung dịch
B. Các ion dương trong dung dịch
C. Các ion dương và ion âm dưới tác dụng của điện trường trong dung dịch
D. Các ion dương và ion âm theo chiều điện trường trong dung dịch
Phát biểu nào sau đây chính xác
Kết quả cuối cùng của quá trình điện phân dung dịch CuSO4 với điện cực bằng đồng là
A. Không có thay đổi gì ở bình điện phân
B. Anôt bị ăn mòn
C. Đồng bám vào catôt
D. Đồng chạy từ anôt sang catôt
Tốc độ chuyển động có hướng của ion \(Na^+\) và \(Cl^-\) trong nước có thể tính theo công thức:\(v = \mu E\), trong đó E là cường độ điện trường, \(\mu\) có giá trị lần lượt là \(4,5.10^{-8} m^2/(V.s)\). Tính điện trở suất của dung dịch NaCl nồng độ 0,1 mol/l, cho rằng toàn bộ các phân tử NaCl đều phân li thành ion.
Người ta muốn bóc một lớp đồng dày \(d = 10 \mu m\) trên một bản đồng diện tích \(S = 1cm^2\) bằng phương pháp điện phân. Cường độ dòng điện là 0,010A. Tính thời gian cần thiết để bóc được lớp đồng. Cho biết đồng có khối lượng riêng là \(p = 8 900 kg/m^3\)
Chọn phát biểu đúng
A. Khi hòa tan axit, bazo hoặc muối vào trong nước, tất cả các phân tử của chúng đều bị phân li thành các ion.
B. Số cặp ion được tạo thành trong dung dịch điện phân không thay đổi theo nhiệt độ
C. Bình điện phân nào cũng có suất phản điện
D. Khi có hiện tượng dương cực tan, dòng điện trong chất điện phân tuân theo định luật Ôm.
Chọn đáp số đúng
Đương lượng điện hóa của niken là k = 3.10-4 g/C. Khi cho một điện lượng 10C chạy qua bình điện phân có anot bằng niken thì khối lượng niken bám vào catot là:
A. 0,3.10-4 g
B. 3.10-3 g
C. 0,3.10-3 g
D. 3.10-4 g
Chiều dày của lớp Niken phủ lên một tấm kim loại là D = 0,05mm sau khi điện phân trong 30 phút. Diện tích mặt phủ của tấm kim loại là 30 cm2. Xác định cường độ dòng điện chạy qua bình điện phân. Cho biết Niken có khối lượng riêng là ρ = 8,9.103kg/m3, A = 58 và n = 2.
Câu nào dưới đây nói về bản chất dòng điện trong chất điện phân là đúng ?
A. Là dòng các êlectron chuyển động có hướng ngược chiều điện trường.
B. Là dòng các ion dương-chuyển động có hướng thuận chiều điện trường.
C. Là dòng các ion âm chuyển động có hướng ngược chiều điện trường.
D. Là dòng chuyển động có hướng đồng thời của các ion dương thuận chiều điện trường và của các ion âm ngược chiều điện trường.
Câu nào dưới đây nói về hiện tượng điện phân có dương cực tan là đúng ?
A. Là hiện tượng điện phân dung dịch axit hoặc bazơ với điện cực là graphit.
B. Là hiện tượng điện phân dung dịch muối có chứa kim loại dùng làm catôt.
C. Là hiện tượng điện phân dung dịch muối có chứa kim loại dùng làm anôt. Kết quả là kim loại tan dần từ anôt tải sang catôt.
D. Là hiện tượng điện phân dung dịch muối có chứa kim loại dùng làm anôt. Kết quả là kim loại được tải dần từ catôt sang anôt.
Một bình điện phân chứa dung dịch muối niken với hai điện cực bằng niken. Xác định khối lượng niken bám vào catôt khi cho dòng điện cường độ I = 5,0 A chạy qua bình này trong khoảng thời gian t = 1 giờ. Đương lượng điện hoá của niken là 0,3.10-3 g/C.
A. 1,5 kg. B. 5,4 g.
C. 1,5 g. D. 5,4 kg.
Một bình điện phân chứa dung dịch đồng sunphat (CuS04) có anôt bằng đồng. Cho dòng điện không đổi chạy qua bình này trong thời gian 30 phút, khi đó khối lượng của catôt tăng thêm 1,143 g. Xác định cường độ dòng điện chạy qua bình điện phân. Đồng (Cu) có khối lượng mol là của A = 63,5 g/mol.
A. 0,965 A. B. 1,93 A.
C. 0,965 mA. D. 1,93 mA.
Một bình điện phân chứa dung dịch bạc nitrat (AgN03) có anôt bằng bạc và điện trở là 2,5 Ω. Hiệu điện thế giữa hai điện cực của bình này là 10 V. Bạc (Ag) có khối lượng mol là A = 108 g/mol và hoá trị n = 1. Xác định khối lượng bạc bám vào catôt sau 16 phút 5 giây.
A. 4,32 g. B. 4,32 kg.
C.2,16g. D. 2,16 kg.
Mắc nối tiếp một bình điện phân chứa dung dịch đồng sunphat (CuSO4) có anôt bằng đồng (Cu) với một bình điện phân chứa dung dịch bạc nitrat (AgNO3) có anôt bằng bạc (Ag). Sau môt khoảng thời gian có dòng điện không đổi chạy qua hai bình này, thì khối lượng anôt của bình chứa dung dịch CuSO4 bị giảm bớt 2,3 g. Xác định khối lượng bạc tới bám vào catôt của bình chứa dung dịch AgNO3. Đồng có khối lượng mol là A1 = 63,5 g/mol và hoá trị n1 = 2, bạc có khối lượng mol là A2 = 108 g/mol và hoá trị n2 = 1. Khối lượng bạc tới bám vào catot của bình chứa dung dịch AgNO3 là
A. 0,67g B. 1,95g
C. 2,66g D. 7,82g
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Bài toán về điện trở Acquy và định luật Faraday.
giúp em 2 bài này với ạ
1. Mắc một vôn kế điện trở rất lớn vào hai cực Acquy thì vôn kế chỉ 20V. Nếu mắc một Ampe kế điện trở R=8Ω vào hai cực Acquy thì Ampe kế chỉ 2A . Tìm điện trở trong của Acquy.
2. Cho mạch điện như hình vẽ: \({\varepsilon _1} = {\varepsilon _2},{\mkern 1mu} {r_1} = {r_2} = 1{\rm{\Omega }},{\mkern 1mu} R = 3{\rm{\Omega }},{\mkern 1mu} C = 100\mu F.\). Bình điện phân đựng dung dịch H2SO4 có sức phản điện ε′=2V , điện trở trong r′=1Ω có các điện cực trơ. Vôn kế V điện trở rất lớn, khóa K điện trở không đáng kể. Khi K ngắt V chỉ 14V . Khi K đóng, tính:
a) Số chỉ V? Điện tích của tụ điện.
b) Khối lượng các hóa chất thoát ra ở điện cực bình điện phân sau 16 phút 5 giây. (Cho O=16;H=1 )
Câu trả lời của bạn
bài này khá khó đấy bạn, hehe
1.
Vôn kế điện trở rất lớn nên ko có dòng chạy trong mạch, số chỉ Vôn kế chính là suất điện động của Ắc-quy.
ε=20(V)
Mắc Ampe kế vào:
\(R + r = \frac{\varepsilon }{I} = \frac{{20}}{2} = 10\)
r=20−R=2(Ω)
ý 2 đây nhé, hehehe, mình thấy các bạn chưa giải
Khi K ngắt, Vôn kế chỉ 14V, suy ra: \({\varepsilon _1} = {\varepsilon _2} = 7(V)\)
Khi K đóng.
Không có dòng qua Vôn kế và tụ C.
Dòng điện trong mạch là:
\(I = \frac{{{\varepsilon _1} + {\varepsilon _2} - \varepsilon '}}{{{r_1} + {r_2} + r' + R}} = 2(A)\)
Số chỉ của V: \({U_V} = {\varepsilon _1} + {\varepsilon _2} - I({r_1} + {r_2}) = 14 - 2 \times 2 = 10(V)\)
Hiệu điện thế 2 đầu tụ: \({U_C} = {U_{NM}} = {\varepsilon _1} - \varepsilon ' - I(r + r') = 1(V)\)
\({Q_C} = UC = 100 \times {10^{ - 6}}(C)\)
Số mol khí H2 thoát ra là:
\(n = \frac{{It}}{{2F}} = \frac{{2 \times 965}}{{2 \times 96500}} = 0.01(mol)\)
Khối lượng H2 thu được:
\({m_{{H_2}}} = 0.01 \times 2 = 0.02(g)\)
Tương tự: \({n_{{O_2}}} = \frac{1}{2}{n_{{H_2}}}\)
cảm ơn các bạn Hoa Hong và Vũ Khúc nhiều nhé !!!!!!!!!!!!!!!!!!!!!!!!!!!
Bài toán về dòng điện trong chất điện phân - Định luật Faraday
Mạch điện như hình vẽ: Bộ nguồn có 15 pin, mỗi pin có \(e = 1,5V;{\mkern 1mu} r = \frac{1}{6}{\rm{\Omega }},{\mkern 1mu} {R_1} = 3{\rm{\Omega }},{\mkern 1mu} {R_3} = {R_4} = 4{\rm{\Omega }},\) , Ampe kế điện trở rất nhỏ,R2R2 là điện trở của bình điện phân đựng dung dịch CuSO4 anod đồng. Biết sau 16 phút 5 giây khối lượng đồng giải phóng ở Katod là 0,48g. . Tính:
a) Cường độ dòng điện qua bình điện phân.
b) Điện trở R2 và số chỉ Ampe kế.
Câu trả lời của bạn
Đang làm nhé. Làm ngắn thì ko hiểu làm dài thì... mệt =.= –
Trước tiên, để đơn giản hóa bài toán.
Ta dùng phương pháp nguồn tương đương:
Xét 6 nguồn mắc song song 6 nguồn.
Độ lớn nguồn tương đương là:
\({\xi _1} = \frac{{6e}}{2} = 3e = 4.5(V)\)
Gọi điện trở tương đương là r1 . Ta có:
\(\frac{{{\xi _1}}}{{{r_1}}} = \frac{{6e}}{{6r}} + \frac{{6e}}{{6r}} = 18 \Rightarrow {r_1} = \frac{{{\xi _1}}}{{18}} = 0.25({\rm{\Omega }})\)
Bây giờ mạch có thể xem là một nguồn (ξ1,r1) nối tiếp với 3 nguồn (e,r)
Nguồn tương đương và điện trở tương đương của hệ này là:
\(\xi = {\xi _1} + 3e = 9(V)\)
\({r_{td}} = {r_1} + 3r = 0.75({\rm{\Omega }})\)
TỨC LÀ, ta có thể thay toàn bộ hệ nguồn song song nối tiếp kia bằng 1 nguồn duy nhất (ξ,rtd)
a) Áp dụng định luật Faraday:
\(0.48 = 64\frac{{{I_2}t}}{{2F}} \Rightarrow {I_2} = \frac{{2 \times 0.48F}}{{64 \times 965}} = 1.5(A)\)
b) Ampe kế điện trở rất nhỏ nên có thể chập điểm M và điểm B.
Mạch trở thành: \({R_1}ss({R_2}nt({R_3}ss{R_4}))\) ss là song song nhé
\({R_{34}} = \frac{{{R_3}}}{2} = 2({\rm{\Omega }})\)
\({U_{34}} = {U_{NB}} = {I_2}{R_{34}} = 1.5 \times 2 = 3(V)\)
Xét 3 đoạn mạch AB, ta có 3 phương trình:
\(\xi - I{r_{td}} = {U_{AB}} \Rightarrow 9 - 0.75I = {U_{AB}}(1)\)
\({I_1}{R_1} = {U_{AB}} \Rightarrow 3{I_1} = {U_{AB}}(2)\)
\({I_2}{R_2} + {U_{NB}} = {U_{AB}} \Rightarrow 1.5{R_2} + 3 = {U_{AB}}(3)\)
Lại có: \(I = {I_1} + {I_2} = {I_1} + 1.5(4)\)
Từ (1), (2), (3), (4), ta giải được:
\({U_{AB}} = 6.3(V)\)
\({R_2} = 2.2({\rm{\Omega }})\)
\({I_1} = 2.1(A)\)
\(I = 3.6(A)\)
Ta có: \({I_4} = \frac{{{U_{34}}}}{{{R_4}}} = \frac{3}{4} = 0.75(A)\)
Xét nút B: \(I = {I_A} + {I_4} \Rightarrow {I_A} = I - {I_4} = 3.6 - 0.75 = 2.85(A)\)
bài này khó quá , huhuhuhuhuhuhuhuhuhuhuhuhuhuhuhu
đúng à khó thật mà sao a biến đổi mạch được hay với
AD cho em hỏi bài này làm ntn đây ạ
Điện phân dung dịch axit sunfuric với các cực platin, ta thu được khí hiđrô và oxi ở các điện cực. Tính thể tích khí thu được ở mỗi điện cực ( ở điều kiện chuẩn) nếu dòng điện qua bình điện phân có cường độ I=5A trong thời gian 1giờ 4 phút 20 giây.
Em cảm ơn nhiều
Câu trả lời của bạn
Hi , trùng hợp quá, bài này mình cũng mới vừa giải xong, nhưng mà tương tự thôi !! ^^
còn dưới đây là bài của bạn nhé
Khối lượng hiđrô thu được ở catốt là:
\({m_1} = \frac{1}{F}\frac{A}{n}.It\)
Thay số A=1,n=1,I=5A,t=3860s
ta được m1=0,2g .
Hiđrô tạo nên ở catôt tồn tại dưới dạng phân tử khí hiđrô.
Ta biết một mol khí hiđrô ( có khối lượng 2g) ở điều kiện chuẩn có thể tích là 22,4 lít=22400 cm3
Vậy thể tích khí hiđrô thu được bằng:
\({V_1} = \frac{{0,2}}{2}22400 = 2240c{m^3}\)
Khối lượng ôxi thu được ở anốt được tính theo công thức tương tự như trên, với A=16,n=2 và bằng m2=1,6g.
Thể tích ôxi thu được bằng:
\({V_2} = \frac{{1.6}}{{32}}.2240 = 1120c{m^3}\)
cái tỉ số này thì tính như thế nào đây cô bác ơi IIIII
Ở nhiệt độ phòng, trong bán dẫn Si tinh khiết, số cặp êlectron-lỗ trống bằng 10−13 số nguyên tử Si . Nếu ta pha P vào Si với tỉ lệ một phần một triệu thì số hạt mang điện tăng lên bao nhiêu lần?
Tỉ số giữa số hạt tải điện khi có tạp chất và khi chưa có tạp chất là:
\(\frac{{{{2.10}^{ - 13}} + {{10}^{ - 6}}}}{{{{2.10}^{ - 13}}}} = 1 + {5.10^6}\)
Tức là số hạt tải điện tăng lên năm triệu lần bạn nhé
Ad có thể đăng giúp em câu này với được không ạ
Chiều dày của một lớp niken phủ lên một tấm kim loại là \(h =0,05mm\) sau khi điện phân trong 30 phút. Diện tích mặt phủ của tấm kim loại là 30 cm2. Xác định cường độ dòng điện chạy qua bình điện phân. Biết niken có \( A = 58,n = 2\) và có khối lượng riêng là \(\rho = 8,9{\rm{ }}g/c{m^3}.\)
Câu trả lời của bạn
Bài này tính I thì bạn cứ thay số vào bình thường nhé! ^^
Ta có : \(m = \rho V = \rho Sh = 1,335{\rm{ }}g\)
Theo công thức Fa-ra-đây:
\(m=\frac{1}{F}.\frac{A}{n}It\)
\(\rightarrow I=\) \(\frac{mFn}{At}\) = 2,47 A.
Câu này tính sao đâu ad ơi, giải chi tiết ra giúp em vs ad nhé!!
Một bình điện phân đựng dung dịch bạc Nitrat với Anốt làm bằng bạc. Điện trở của bình điện phân là \(R = 2\Omega \) . Hiệu điện thế đặt ở hai cực là \(U = 10(V)\). Cho \(A = 108, n = 1\). Khối lượng bạc bám vào cực âm sau 2 giờ là
Câu trả lời của bạn
Ơ bài này đơn giản lắm bn
Dòng điện qua bình :
\(I = \frac{U}{R} = 5(A)\)
Công thức pha-ra-đây về điện phân :
\(m = \frac{1}{F}.\frac{A}{n}q = 40,3(g)\)
Thế còn đề cho như này thì tính sao đây ạ ???????????????
Hai bình điện phân: \((FeC{l_3}/Fe\) và CuSO4/Cu) mắc nối tiếp. Sau một khoảng thời gian, bình thứ nhất giải phóng một lượng sắt là 1,4 g. Tính lượng đồng giải phóng ở bình thứ hai trong cùng khoảng thời gian đó. Biết nguyên tử lượng của đồng và sắt là 64 và 56, hóa trị của đồng và sắt là 2 và 3.
2222!!
bài của bn Bo Bo tính từng bước là ra thôi nhé, ko phải lăn tăn gì đâu
Theo công thức Fa-ra-đây:
Khối lượng sắt giải phóng ở bình thứ nhất:
\({m_1} = \frac{1}{F}.\frac{{{A_1}}}{{{n_1}}}It\)
Khối lượng đồng giải phóng ở bình thứ hai:
\(\begin{array}{l}
{m_2} = \frac{1}{F}.\frac{{{A_2}}}{{{n_2}}}It\\
\to \frac{{{m_2}}}{{{m_1}}} = \frac{{{A_2}{n_1}}}{{{A_1}{n_2}}}{m_1} \to {m_2} = 2,4g
\end{array}\)



Hướng dẫn giúp em câu này được không ạ >>
Người ta muốn bóc một lớp đồng dày \(d = 10 \mu m\) trên một bản đồng diện tích \(S = 1cm^2\) bằng phương pháp điện phân. Cường độ dòng điện là 0,010A. Tính thời gian cần thiết để bóc được lớp đồng. Cho biết đồng có khối lượng riêng là \(p = 8 900 kg/m^3\)
Câu trả lời của bạn
Có thể giúp e bài này được không ạ ?
Để tách đồng ra khỏi một hỗn hợp rắn chứa 12% tạp chất khác người ta dùng thanh hỗn hợp này làm cực dương của bình điện phân đựng dung dịch \(CuS{O_4}.\) .Hiệu điện thế giữa hai cực là \(U = 6(V)\). Tính điện năng tiêu hao để xử lý \(1 (kg)\) hỗn hợp ?
Hi Trang, mình thấy bài này cũng khá đơn giản ^^
Khối lượng đồng có trong thanh :
\({m_{Cu}} = \frac{{(100 - 12)}}{{100}}m = 0,88(kg)\)
Định luật Faraday :
\(\begin{array}{l}
m = \frac{1}{F}.\frac{A}{n}q\\
\Leftrightarrow 880 = \frac{1}{{96500}}.\frac{{64}}{2}q \Rightarrow q = {2654.10^3}(C)
\end{array}\)
Điện năng tiêu hao để xử lý \(1 (kg)\) hỗn hợp :
\(W = qU = {2654.10^3}.6 = 15923{\rm{ }}\left( {kJ} \right) = 4,42\left( {kWh} \right)\)
dạ, cho em hỏi câu điện trở suất này luôn mn ơi . ^^^^^
Tốc độ chuyển động có hướng của ion \(Na^+\) và \(Cl^-\) trong nước có thể tính theo công thức:\(v = \mu E\), trong đó E là cường độ điện trường, \(\mu\) có giá trị lần lượt là \(4,5.10^{-8} m^2/(V.s)\). Tính điện trở suất của dung dịch NaCl nồng độ 0,1 mol/l, cho rằng toàn bộ các phân tử NaCl đều phân li thành ion.
Giúp em vs nhé
^^
Câu Điện trở suất của bạn Ngạn đây nhé ;
Mật độ của các ion \(Na^+\) và \(Cl^-\):
\(N = 0,1.1000.6,023.10^{23} = 6,023.10^{25}/m^3\)
Điện dẫn suất của dung dịch:
\(\sigma = 1,{6.10^{ - 19}}.6,{023.10^{25}}.(4,5 + 6,8){.10^{ - 8}} = 1,088{(\Omega /m)^{ - 1}}\)
⇒ Điện trở suất \(\rho =\frac{1}{\sigma }=\frac{1}{1,088}=0,92\Omega .m\)
Good luck , hehe
em cũng có 1 câu tính thời gian điện phân các anh chị ơii, đề bài yêu cầu chỉ cần tính thời gian thôi ạ
Cho một mạch điện gồm có một nguồn điện \(( = 4V;r = 0,2{\rm{\Omega }})\) cung cấp dòng điện cho một bình điện phân đựng dung dịch CuSO4 với anôt làm bằng plantin. Biết suất phản điện và điện trở của bình điện phân ϵ′=2V,r′=1,8Ω và lượng đồng bám vào catốt là m=1,2g . Tính thời gian điện phân?
Bài của bn Hải Yến để mình ra tay nhé, hehe
Thân chào !!!
Hi. bài này áp dụng công thức Fa-ra-day để tìm khối lượng Cu trước bạn nhé.
Ta có:
Khối lượng đồng phải bóc đi là: \(m = 8 900.1.10^{-4}.10.10^{-6} = 8,9.10^{-6} kg\)
Theo công thức Fa-ra-đây: m = ; suy ra t =
Với A = 64g = 6,4.10-2kg; n = 2; I = 10-2 A, suy ra:
t = = 2 683,9 s
Vì sao người ta thường xuyên kiểm tra và đổ nước thêm cho các ắcquy của xe máy, xe ôtô?
Câu trả lời của bạn
Khi nạp điện cho ắc qui, nước bị phân tích thành hiđrô và oxi, còn axit không đổi, do đó nồng độ dung dịch tăng dần, lượng nước giảm dần, không những dung dịch càng trở nên đậm đặc hơn có hại cho ắc qui mà các cực lại không được nhúng ngập hết trong dung dịch, khả năng tích điện sẽ giảm.
Vì vậy khi sử dụng ắc qui cần kiểm tra mức dung dịch để đổ thêm nước cho kịp thời.
Điện phân cực dương tan một dung dịch trong 20 phút thì khối lượng cực âm tăng thêm 2g. Nếu điện phân dung dịch đó (trong cùng điều kiện) trong thời gian một giờ thì khối lượng cực âm tăng thêm là?
Câu trả lời của bạn
Quá trình điện phân sunphát đồng sẽ tiếp tục cho đến lúc nào, nếu dùng các điện cực bằng than? nếu dùng các điện cực bằng đồng?
Câu trả lời của bạn
Với các điện cực bằng than - tiếp tục cho đến lúc tất cả các ion đồng thoát ra khỏi dung dịch (khi đó trong bình còn lại axit sunfuric). Với các cực bằng đồng - cho đến khi anôt bị hoà tan.
Tại sao xung quanh chất điện phân, chẳng hạn xung quanh dung dịch muối ăn, lại không có điện trường và chúng ta cho rằng nó không tích điện, mặc dầu trong nó có các ion mang điện?
Câu trả lời của bạn
Vì trong mỗi đơn vị thể tích chất điện phân có bao nhiêu điện tích dương thì cũng có bấy nhiêu điện tích âm và trường của chúng ở ngoài chất điện phần bù trừ lẫn nhau. Bởi vậy toàn bộ chất điện phân giống như là một vật không tích điện.
Có thể dựa vào hình dạng bên ngoài của các bản trong acqui axit để xác định bản nào là dương bản nào là âm được không?
Câu trả lời của bạn
Người ta đưa một nam châm vào một vòng bằng chất điện môi. Có hiện tượng gì xảy ra?
Câu trả lời của bạn
Sự phân cực của chất điện môi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *