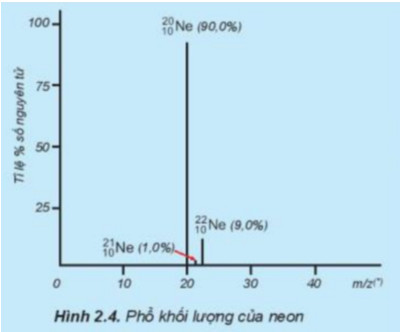
Tỉ lệ phần trăm số nguyên tử các đồng vị của neon (Ne) được xác định theo phổ khối lượng (Hình 2.4). Tính nguyên tử khối trung bình của Ne.
Hướng dẫn giải
- Nguyên tử khối trung bình của một nguyên tố hóa học ghi trong bảng tuần hoàn là nguyên tử khối trung bình của các đồng vị trong tự nhiên.
- Nguyên tử khối trung bình: \(M = \frac{{aA + bB + cC + {\text{dD}} + ...}}{{100}}\)
Trong đó:
A, B, C, D… là số khối của các đồng vị
a, b, c, d… là phần trăm của các đồng vị tương ứng
Lời giải chi tiết
Ta có: \({}^{20}Ne\)chiếm 90,0%; \(^{21}Ne\)chiếm 1,0%; \({}^{22}Ne\)chiếm 9,0%
→ \({M_{Ne}} = \frac{{90.20 + 1.21 + 9.22}}{{100}} = 20,19\)
Vậy nguyên tử khối trung bình của Ar là 20,19
-- Mod Hóa Học 10