1. Tính tốc độ trung bình của phản ứng (4) theo O2 trong 100 giây đầu tiên
2. Từ Bảng 16.1, có thể tính được tốc độ trung bình của phản ứng sau 50 giây hay không? Vì sao?
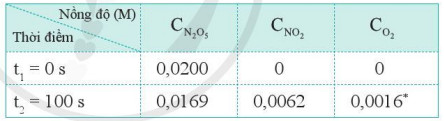
Bảng 16.1. Dữ liệu nồng độ các chất (molL-1)
Phương pháp giải
Áp dụng công thức:
\(\overline v = - \frac{1}{a}.\frac{{\Delta {C_A}}}{{\Delta t}} = - \frac{1}{b}.\frac{{\Delta {C_B}}}{{\Delta t}} = \frac{1}{m}\frac{{\Delta {C_M}}}{{\Delta t}} = \frac{1}{n}\frac{{\Delta {C_N}}}{{\Delta t}}\)
Lời giải chi tiết
1. Ta có: O2 là chất sản phẩm \(v = \frac{1}{n}.\frac{{\Delta {C_{{O_2}}}}}{{\Delta t}}\)
Trong đó: C sau = 0,0016M, C trước = 0M → \({\Delta C}\) = 0,0016 - 0 = 0,0016M
→ n = 1 → \({\Delta t}\) = 100s
Tốc độ trung bình của phản ứng theo O2 trong 100 giây đầu tiên là: \(v = \frac{{0,00116}}{{100}} = 1,{6.10^{ - 5}}(M/s)\)
2.
- Nồng độ biến thiên chất không đồng đều sau mỗi khoảng đơn vị thời gian
→ Ta không thể tính được nồng độ các chất sau 50 giây
→ Không tính được tốc độ trung bình của phản ứng sau 50 giây
-- Mod Hóa Học 10