Hãy dự đoán xu hướng nhường, nhận electron của mỗi nguyên tử trong từng cặp nguyên tử sau. Vẽ mô hình (hoặc viết số electron theo lớp) quá trình các nguyên tử nhường, nhận electron để tạo ion
a) K (Z = 19) và O (Z = 8).
b) Li (Z = 3) và F (Z = 9).
c) Mg (Z = 12) và P (Z = 15)
Phương pháp giải
- Các kim loại có 1, 2 hoặc 3 electron ở lớp ngoài cùng có xu hướng nhường bớt toàn bộ các electron này để tạo thành ion dương
- Các phi kim với 5, 6 hoặc 7 electron ở lớp ngoài cùng có xu hướng nhận thêm electron để đạt 8 electron ở lớp ngoài cùng
Lời giải chi tiết
a)
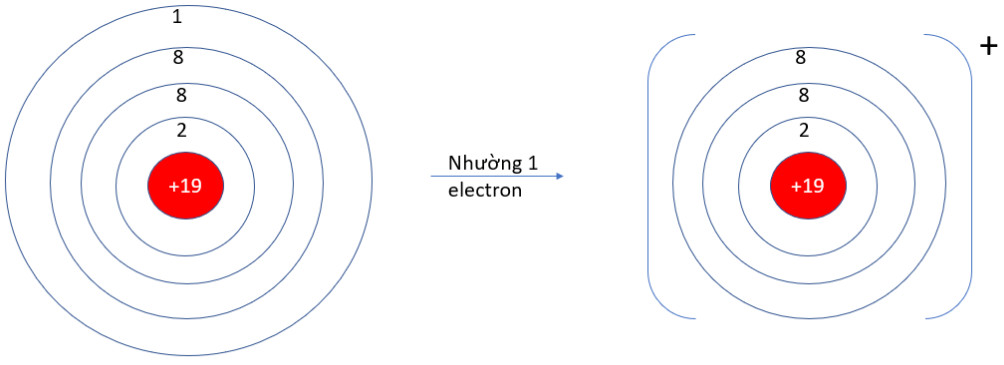
- K (Z = 19): 1s22s22p63s23p64s1 → Có 1 electron ở lớp vỏ ngoài cùng → Xu hướng nhường 1 electron
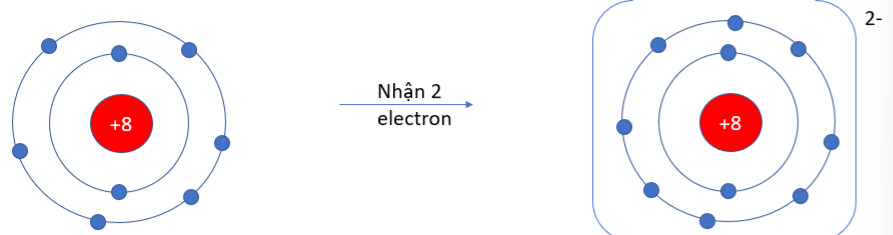
- O (Z = 8): 1s22s22p4 → Có 6 electron ở lớp vỏ ngoài cùng → Xu hướng nhận 2 electron
b)
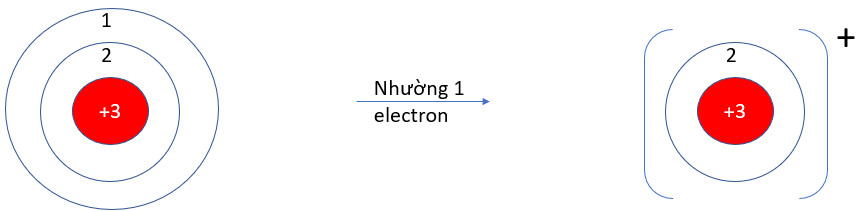
- Li (Z = 3): 1s22s1 → Có 1 electron ở lớp vỏ ngoài cùng → Xu hướng nhường 1 electron
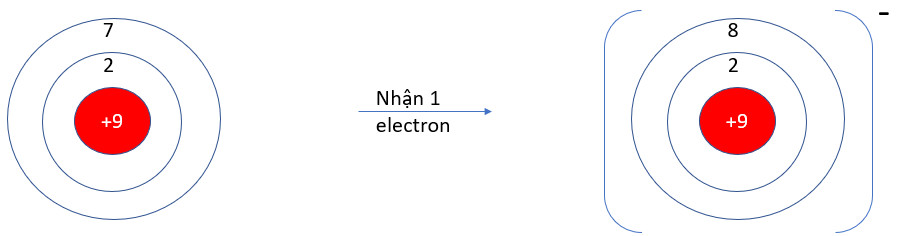
- F (Z = 9): 1s22s22p5 → Có 7 electron ở lớp vỏ ngoài cùng → Xu hướng nhận 1 electron
c)
- Mg (Z = 12): 1s22s22p63s2 → Có 2 electron ở lớp vỏ ngoài cùng → Xu hướng nhường 2 electron
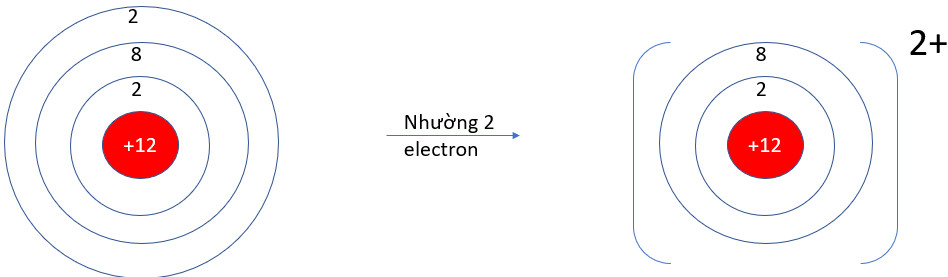
- P (Z = 15): 1s22s22p63s23p3 → Có 5 electron ở lớp vỏ ngoài cùng → Xu hướng nhận 3 electron
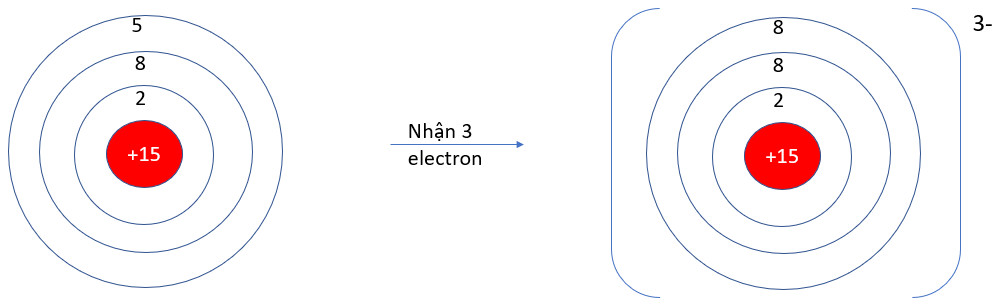
-- Mod Hóa Học 10