Bảng tuần hoàn có nguyên tắc sắp xếp và cấu tạo như thế nào ? Để biết chi tiết, DapAnHay xin chia sẻ với các bạn Bài 4: Sơ lược về bảng tuần hoàn các nguyên tố hóa học môn Khoa học tự nhiên 7 SGK Kết nối tri thức. Với kiến thức trọng tâm và các bài tập có lời giải chi tiết, hi vọng rằng đây sẽ là tài liệu giúp các bạn học tập tốt hơn.
- Năm 1869, Men-đê-lê-ép (D. I. Mendeleev) (1834 - 1907), nhà bác học người Nga đã xây dựng bảng tuần hoàn các nguyên tố hoá học theo chiều tăng dần khối lượng nguyên tử. Sau đó, các nhà khoa học đã chứng minh rằng điện tích hạt nhân nguyên tử mới là cơ sở để xây dựng bảng tuần hoàn các nguyên tố hoá học.
- Ngày nay, bảng tuần hoàn các nguyên tố hoá học (gọi tắt là bảng tuần hoàn) gồm 118 nguyên tố hoá học, được xây dựng theo nguyên tắc sau:
+ Các nguyên tố hoá học được xếp theo chiều tăng dần của điện tích hạt nhân.
+ Các nguyên tố trong cùng một hàng có cùng số lớp electron trong nguyên tử.
+ Các nguyên tố trong cùng cột có tính chất gần giống nhau.
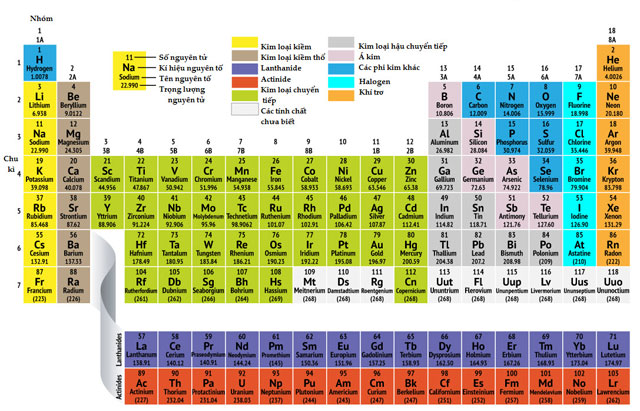
Bảng tuần hoàn các nguyên tố hóa học
| - Các nguyên tố hoá học trong bảng tuần hoàn được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử. - Các nguyên tố cùng chu kì có cùng số lớp electron, các nguyên tố cùng nhóm có tính chất gần giống nhau. |
|---|
a. Ô nguyên tố
- Mỗi nguyên tố hoá học được xếp vào một ô của bảng tuần hoàn, gọi là ô nguyên tố.
- Ô nguyên tố cho biết: kí hiệu hoá học, tên nguyên tố, số hiệu nguyên tử và khối lượng nguyên tử của nguyên tố đó.
- Số hiệu nguyên tử = Số đơn vị điện tích hạt nhân = Số electron trong nguyên tử.
- Số hiệu nguyên tử chính là số thứ tự của nguyên tố trong bảng tuần hoàn.
Ví dụ: Các thông tin về nguyên tố ở ô số 8 trong bảng tuần hoàn được chỉ ra trong Hình 4.2.
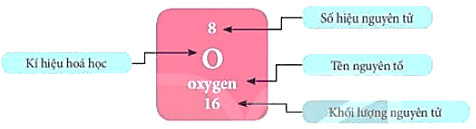
Hình 4.2. Ô nguyên tố oxygen
b. Chu ki
- Chu kì là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron và được xếp theo chiều điện tích hạt nhân tăng dần khi đi từ trái qua phải.
- Bảng tuần hoàn hiện nay gồm 7 chu kì được đánh số từ 1 đến 7, mỗi chu kì là 1 hàng ngang (riêng chu kì 6 và chu kì 7, mỗi chu kì có thêm 1 hàng xếp tách riêng cuối bảng).
- Chu kì 1, 2, 3 được gọi là các chu kì nhỏ, chu kì 4, 5, 6, 7 được gọi là các chu kì lớn. Ví dụ: Chu kì 1 gồm 2 nguyên tố là H và He, chu kì 2 gồm 8 nguyên tố từ Li đến Ne và chu kì 3 gồm 8 nguyên tố từ Na đến Ar (xem Hình 4.3).
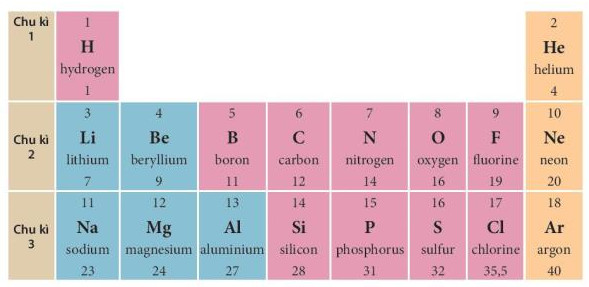
Hình 4.3. Các nguyên tố thuộc ba chu kì đầu tiên của bảng tuần hoàn
- Trong bảng tuần hoàn, số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố trong chu kì đó.
c. Nhóm
- Bảng tuần hoàn gồm 8 nhóm A được đánh số từ IA đến VIIIA và 8 nhóm B được đánh số từ IB đến VIIIB.
- Các nguyên tố trong cùng một nhóm A có số electron ở lớp ngoài cùng bằng nhau (trừ trường hợp nguyên tố He), do vậy chúng có tính chất gần giống nhau.
- Trong cùng một nhóm, khi đi từ trên xuống dưới, điện tích hạt nhân của nguyên tử các nguyên tố tăng dần.
Ví dụ:
- Nhóm IA gồm 7 nguyên tố từ H đến Fr (xem Hình 4.5a). Các nguyên tố trong nhóm IA là các kim loại điển hình (trừ H).
- Nhóm VIIA gồm 6 nguyên tố từ 1 đến Ts (xem Hình 4.5b). Các nguyên tố trong nhóm VIIA là các phi kim điển hình (trừ Ts).

a) b)
Hình 4.5. Các nguyên tố thuộc nhóm IA và nhóm VIIA của bảng tuần hoàn
- Số thứ tự của nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong nhóm đó.
| Cấu trúc bảng tuần hoàn gồm các ô nguyên tố, chu kì và nhóm. |
|---|
a. Các nguyên tố kim loại
- Trong số 118 nguyên tố hoá học đã biết có hơn 90 nguyên tố là kim loại. Trong bảng tuần hoàn, các nguyên tố kim loại ở góc dưới bên trái của bảng và được thể hiện bằng màu xanh (xem Bảng tuần hoàn trang 25). Chúng gồm:
+ Hầu hết các nguyên tố thuộc nhóm IA, nhóm IIA, nhóm IIIA và một số nguyên tố các nhóm IVA, VA, VIA.
+ Các nguyên tố thuộc nhóm IB đến VIIIB, các nguyên tố lanthanide và các nguyên tố actinide được xếp riêng thành hai hàng ở cuối bảng.
- Một số nguyên tố kim loại thông dụng và ứng dụng của chúng trong đời sống được chỉ ra trong Hình 4.6.
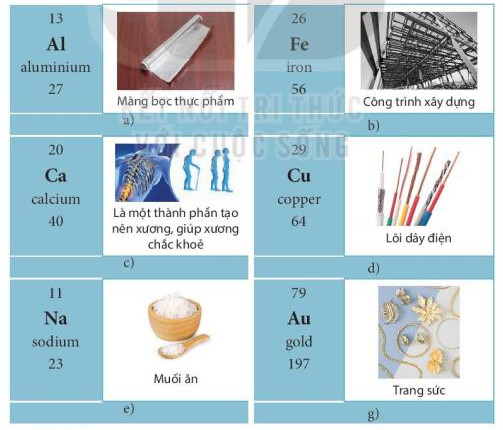
Hình 4.6. Ứng dụng của một số nguyên tố kim loại thông dụng trong đời sống
b. Các nguyên tố phi kim
- Một số phi kim rất quen thuộc trong đời sống của chúng ta như: oxygen là phi kim không thể thiếu với sự sống của hầu hết sinh vật, được tạo ra trong quá trình quang hợp và được sử dụng trong quá trình hô hấp; chlorine có thể được dùng để khử trùng nước sinh hoạt.
- Trong số 118 nguyên tố hoá học đã biết, có chưa đến 20 nguyên tố là phi kim. Ở điều kiện thường, chúng có thể ở thể rắn, thể lỏng hay thể khí (xem Hình 4.7). Trong bảng tuần hoàn, các nguyên tố phi kim chủ yếu ở góc trên bên phải của bảng, được thể hiện bằng màu hồng. Chúng gồm:
+ Hầu hết các nguyên tố thuộc nhóm VIIA, VIA, VA.
+ Một số nguyên tố thuộc nhóm IVA, IIIA.
+ Nguyên tố H nhóm IA.

a) Nguyên tố O, S thuộc nhóm VIA b) Nguyên tố Cl, Br thuộc nhóm VIIA
Hình 4.7. Trạng thái, màu sắc của một số phi kim ở nhiệt độ thường
c. Các nguyên tố khí hiếm
- Trong số 118 nguyên tố đã biết có 7 nguyên tố là nguyên tố khí hiểm. Nguyên tử của chúng có lớp electron ngoài cùng bền vững nên khó bị biến đổi hoá học. Một số ứng dụng trong đời sống của khí hiếm như: Hệ được sử dụng trong khinh khí cầu, Ne được dùng trong đèn LED,...
- Trong bảng tuần hoàn, nguyên tố khí hiếm nằm ở nhóm VIIIA và được thể hiện bằng màu vàng.
| - Trong bảng tuần hoàn, các nguyên tố kim loại tập trung ở các nhóm IA, IIA, IIIA và các nhóm B. - Các nguyên tố phi kim tập trung ở các nhóm VA, VIA, VIIA, còn các nguyên tố khí hiếm ở nhóm VIIIA. |
|---|
Bài 1: Ngày nay, người ta đã xác định được hàng chục triệu chất hóa học với các tính chất khác nhau được tạo thành từ hơn một trăm nguyên tố hóa học. Liệu có nguyên tắc nào sắp xếp các nguyên tố để dễ nhận ra tính chất của chúng không?
Hướng dẫn giải
- Nguyên tắc sắp xếp các nguyên tố để dễ dàng nhận ra tính chất của chúng
+ Các nguyên tố hóa học được xếp theo chiều tăng dần của điện tích hạt nhân
+ Các nguyên tố trong cùng một hàng có cùng số lớp electron trong nguyên tử
+ Các nguyên tố trong cùng cột có tính chất gần giống nhau
Bài 2: Số hiệu nguyên tử của một nguyên tố hóa học cho biết những thông tin gì về nguyên tố đó?
Hướng dẫn giải
- Số hiệu nguyên tử = số đơn vị điện tích hạt nhân = số proton trong hạt nhân = số electron trong nguyên tử = số thứ tự của nguyên tố trong bảng tuần hoàn
- Ví dụ: Nguyên tử hydrogen có số hiệu nguyên tử là 1
→ Nguyên tố hydrogen ở ô số 1 trong bảng tuần hoàn, điện tích hạt nhân là +1 (do có 1 proton trong hạt nhân) cà có 1 electron trong nguyên tử
Bài 3: Quan sát bảng tuần hoàn, cho biết số hiệu nguyên tử, số lớp electron lần lượt của nguyên tử carbon (C) và nhôm (Al). Hai nguyên tố đó nằm ở chu kì nào trong bảng tuần hoàn?
Hướng dẫn giải
- Nguyên tố carbon:
+ Có số hiệu nguyên tử: 6
+ Nằm ở chu kì 2 → Có 2 lớp electron
- Nguyên tố nhôm:
+ Có số hiệu nguyên tử: 13
+ Nằm ở chu kì 3 →Có 3 lớp electro
Học xong bài học này, em có thể:
- Nêu được các nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hoá học.
- Mô tả được cấu tạo bảng tuần hoàn gồm ô, nhóm, chu kì.
- Sử dụng được bảng tuần hoàn để chỉ ra các nhóm nguyên tố kim loại, phi kim, khí hiếm.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Khoa học tự nhiên 7 Kết nối tri thức Bài 4 cực hay có đáp án và lời giải chi tiết.
Nhóm các nguyên tố được sắp xếp theo chiều tính phi kim tăng dần là
Dãy các kim loại nào sau đây được sắp xếp theo chiều tính kim loại tăng dần ?
Cho các nguyên tố sau O, P, N. Hãy chỉ ra thứ tự sắp xếp đúng theo chiều tính phi kim tăng dần
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Khoa học tự nhiên 7 Kết nối tri thức Bài 4để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Hoạt động trang 23 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải câu hỏi 1 trang 24 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải câu hỏi 2 trang 24 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải câu hỏi trang 26 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Hoạt động trang 27 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải câu hỏi trang 27 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Hoạt động trang 28 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải câu hỏi trang 29 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải câu hỏi 1 trang 30 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải câu hỏi 2 trang 30 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải câu hỏi 1 trang 31 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải câu hỏi 2 trang 31 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Giải câu hỏi 3 trang 31 SGK Khoa học tự nhiên 7 Kết nối tri thức - KNTT
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Nhóm các nguyên tố được sắp xếp theo chiều tính phi kim tăng dần là
Dãy các kim loại nào sau đây được sắp xếp theo chiều tính kim loại tăng dần ?
Cho các nguyên tố sau O, P, N. Hãy chỉ ra thứ tự sắp xếp đúng theo chiều tính phi kim tăng dần
Biết X có cấu tạo nguyên tử như sau: điện tích hạt nhân là 12+, có 3 lớp electron, lớp ngoài cùng có 2 electron. Vị trí của X trong bảng tuần hoàn là
Nguyên tử của nguyên tố X có 3 lớp electron, lớp electron ngoài cùng có 7 electron. Vị trí và tính chất cơ bản của nguyên tố X là
Nguyên tố M có số hiệu nguyên tử là 19, chu kỳ 4, nhóm I trong bảng tuần hoàn các nguyên tố hóa học. Phát biểu nào sau đây đúng ?
Nguyên tố X ở chu kỳ 4 nhóm VI, nguyên tố Y ở chu kỳ 2 nhóm VII. So sánh tính chất của X và Y thấy
Chọn đáp án sai?
Cho điện tích hạt nhân nguyên tử X là 15+. Biết trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện là 14. Xác định nguyên tố X và số hạt nơtron của X.
Nguyên tử A có tổng số hạt proton, nơtron và electron là 28, trong đó số hạt mang điện gấp 1,8 lần số hạt không mang điện. A là
Sắp xếp các nguyên tố hóa học
Chuẩn bị:
- 18 thẻ ghi thông tin của 18 nguyên tố đầu tiện theo mẫu trong Hình 4.1.

Tiến hành: gắn các thẻ vào bảng mẫu ở trên từ trái qua phải, từ trên xuống dưới, mỗi thẻ vào 1 ô theo chiều tăng dần số đơn vị điện tích hạt nhân của các nguyên tố.
Thảo luận nhóm và nhận xét về các đặc điểm của bảng sau khi đã sắp xếp:
1. Sự thay đổi số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong một hàng khi đi từ trái sang phải
2. Số electron ở lớp ngoài cùng của nguyên tử các nguyên tố trong cùng một cột
Dựa vào đặc điểm nào về cấu tạo nguyên tử để sắp xếp các nguyên tố vào hàng, vào cột trong bảng tuần hoàn?
Sử dụng bảng tuần hoàn, hãy cho biết các nguyên tố nào trong số các nguyên tố Li, Na, C, O có cùng số lớp electron trong nguyên tử?
1. Quan sát Hình 4.2, cho biết số proton, electron trong nguyên tử oxygen

Hình 4.2. Ô nguyên tố oxygen
2. Sử dụng bảng tuần hoàn và cho biết kí hiệu hóa học, tên nguyên tố, số hiệu nguyên tử, khối lượng nguyên tử và số electron trong nguyên tử của các nguyên tố ở ô số 6, 11
Tìm hiểu mối quan hệ giữa số lớp electron của nguyên tử các nguyên tố với số thứ tự của chu kì
Chuẩn bị: 6 mô hình sắp xếp electron ở vỏ nguyên tử của sáu nguyên tố H, He, Li, Be, C, N theo mẫu được mô tả trong Hình 4.4
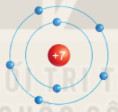
Hình 4.4. Mô hình sắp xếp các electron ở vỏ nguyên tử nitrogen
Quan sát các mô hình đã chuẩn bị, thảo luận và thực hiện các yêu cầu sau:
1. Hãy cho biết số lớp electron của nguyên tử các nguyên tố trên.
2. So sánh số lớp electron của nguyên tử các nguyên tố trên với số thứ tự chu kì của các nguyên tố đó.
1. Quan sát Hình 4.3 và cho biết tên, kí hiệu hóa học và điện tích hạt nhân của nguyên tử các nguyên tố xung quanh nguyên tố carbon

Hình 4.3. Các nguyên tố thuộc ba chu kì đầu tiên của bảng tuần hoàn
2. Hãy cho biết số lớp electron của nguyên tử các nguyên tố thuộc chu kì 3. Giải thích
Tìm hiểu mối quan hệ giữa số electron ở lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự của nhóm
Chuẩn bị: 4 mô hình sắp xếp electron ở vỏ nguyên tử của Li, Na, F, Cl theo mẫu mô tả trong Hình 4.4.
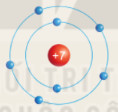
Hình 4.4. Mô hình sắp xếp các electron ở vỏ nguyên tử nitrogen
Quan sát các mô hình đã chuẩn bị, thảo luận và trả lời câu hỏi:
1. Hãy cho biết nguyên tử các nguyên tố nào có cùng số electron ở lớp ngoài cùng
2. Hãy so sánh số electron lớp ngoài cùng của nguyên tử các nguyên tố với số thứ tự nhóm của các nguyên tố đó
Sử dụng bảng tuần hoàn, hãy cho biết:
1. Số electron lớp ngoài cùng của nguyên tử hai nguyên tố Al và S. Giải thích
2. Hãy kể tên nguyên tố thuộc chu kì nhỏ và cùng nhóm với nguyên tố beryllium
1. Sử dụng bảng tuần hoàn, hãy xác định vị trí (số thứ tự, chu kì, nhóm) của các nguyên tố Al, Ca, Na.
2. Tính chất nào của nhôm, sắt, đồng đã được dùng trong các ứng dụng ở trong Hình 4.6?

Hình 4.6. Ứng dụng của một số nguyên tố kim loại thông dụng trong đời sống
Sử dụng bảng tuần hoàn, hãy xác định vị trí (số thứ tự, chu kì, nhóm) của các nguyên tố có tên trong Hình 4.7

a) Nguyên tố O, S thuộc nhóm VIA b) Nguyên tố Cl, Br thuộc nhóm VIIA
Hình 4.7. Trạng thái, màu sắc của một số phi kim ở nhiệt độ thường
Sử dụng bảng tuần hoàn, hãy xác định vị trí (số thứ tự, chu kì, nhóm) của khí hiếm neon
Bảng tuần hoàn các nguyên tố hóa học gồm các nguyên tố:
A. Kim loại và phi kim
B. Phi kim và khí hiếm
C. Kim loại và khí hiếm
D. Kim loại, phi kim và khí hiếm
Hãy chọn đáp án đúng nhất.
Cho các nguyên tố sau:

a) Sử dụng bảng tuần hoàn, hãy cho biết trong các nguyên tố trên, nguyên tố nào là kim loại, nguyên tố nào là phi kim
b) Nêu ứng dụng trong đời sống của một nguyên tố trong số các nguyên tố trên
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi
Câu trả lời của bạn
- Các nguyên tố B, C, O và F được xếp vào cùng 1 hàng (chu kì 2) vì cả 5 nguyên tố này đều có 2 lớp electron trong nguyên tử.
- Tương tự, các nguyên tố Na, Mg và Al được xếp vào cùng 1 hàng (chu kì 3) vì nguyên tử của các nguyên tố này đều có 3 lớp electron.
Cho những phát biểu sau:
a) Khối lượng của một nguyên tử bằng tổng số proton của nguyên tử đó.
b) Tất cả nguyên tử của các nguyên tố nhóm VA đều có 5 electron ở lớp ngoài cùng.
c) Tất cả nguyên tử của các nguyên tố ở chu kì II đều có 2 electron ở lớp ngoài cùng.
d) Trong nguyên tử, các electron được xếp theo từng lớp. Các electron được sắp xếp lần lượt vào các lớp theo chiều từ gần hạt nhân ra ngoài. Mỗi lớp electron có một số electron nhất định.
e) Số thứ tự của nhóm bằng số lớp electron trong nguyên tử của các nguyên tố thuộc nhóm đó.
g) Số thứ tự của chu kì bằng số lớp electron trong nguyên tử của các nguyên tố thuộc chu kì đó.
Số phát biểu đúng là
Câu trả lời của bạn
Các phát biểu b, d, g đúng.
Cho biết một nguyên tử của nguyên tố X có điện tích hạt nhân là +17. Hãy chọn câu đúng trong các câu sau:
A. Nguyên tố X ở chu kì 3, nhóm VIIA; là phi kim; có 17 proton, 7 electron.
B. Nguyên tố X ở chu kì 3, nhóm VIIA; là phi kim; có 17 proton, 17 electron.
C. Nguyên tố X ở chu kì 2, nhóm VIIA; là kim loại; có 17 proton, 17 electron.
D. Nguyên tố X ở chu kì 2, nhóm VIIA; là phi kim; có 17 proton, 7 electron.
Câu trả lời của bạn
Đáp án đúng là: B
- X có điện tích hạt nhân là +17 nên nguyên tử X có 17 proton và 17 electron (loại đáp án A và D).
- X có 17 electron được phân vào 3 lớp, vậy X thuộc chu kì 3 (loại đáp án C).
Cho biết các nguyên tử của nguyên tố M có 3 lớp electron và có 1 electron ở lớp ngoài cùng. Nguyên tố M có vị trí trong bảng tuần hoàn như sau:
A. ô số 9, chu kì 3, nhóm IA.
B. ô số 10, chu kì 2, nhóm IA.
C. ô số 12, chu kì 3, nhóm IA.
D. ô số 11, chu kì 3, nhóm IA.
Câu trả lời của bạn
M có 3 lớp electron nên thuộc chu kì 3 ⇒ Loại đáp án B.
M có 1 electron ở lớp ngoài cùng nên thuộc nhóm IA.
M có 3 lớp electron trong đó: lớp thứ nhất có 2 electron, lớp thứ hai có 8 electron, lớp thứ 3 có 1 electron ⇒ M có 11 electron. Vậy M thuộc ô 11 trong bảng tuần hoà
=> Đáp án đúng là: D
Biết một nguyên tử của nguyên tố X có điện tích hạt nhân là +8. Hãy dự đoán vị trí của X trong bảng tuần hoàn. Cho biết tên của nguyên tố đó. X là nguyên tố kim loại, phi kim hay khí hiếm?
Câu trả lời của bạn
- Nguyên tử nguyên tố X có điện tích hạt nhân là +8 nên số hiệu nguyên tử X là 8.
Vậy X thuộc ô nguyên tố có số thứ tự là 8, chu kì 2 (vì có 2 lớp electron), nhóm VIA (vì có 6 electron ở lớp ngoài cùng).
- Nguyên tố X là nguyên tố oxygen, là nguyên tố phi kim.
A. Bảng tuần hoàn gồm 3 chu kì nhỏ và 4 chu kì lớn.
B. Số thứ tự của chu kì bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố thuộc chu kì đó.
C. Số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố thuộc chu kì đó.
D. Các nguyên tố trong cùng chu kì được sắp xếp theo chiều điện tích hạt nhân tăng dần.
Câu trả lời của bạn
B. Số thứ tự của chu kì bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố thuộc chu kì đó.

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *