Nội dung Bài tập (Chủ đề 1,2) chương trình Khoa học tự nhiên lớp 7 SGK Cánh diều được DapAnHay biên soạn sẽ giúp các em củng cố các kiến thức về nguyên tử, nguyên tố hóa học, bảng tuần hoàn các nguyên tố hóa học. Mời các em cùng tham khảo nội dung chi tiết trong bài giảng sau đây.
Ôn tập nội dung kiến thức Bài 1: Nguyên tử
- Nguyên tử: là những hạt cực kì nhỏ bé, không mang điện, cấu tạo nên chất.
- Cấu tạo nguyên tử:
+ Vỏ nguyên tử
+ Hạt nhân nguyên tử
- Sự chuyển động của electron trong nguyên tử: electron phân bố trên các lớp electron và chuyển động quanh hạt nhân nguyên tử trên những quỹ đạo xác định.
- Khối lượng nguyên tử: bằng tổng khối lượng của proton và neutron có trong nguyên tử, được tính bằng đơn vị amu.
Ôn tập nội dung kiến thức Bài 2: Nguyên tố hóa học
- Nguyên tố hoá học: là tập hợp những nguyên tử có cùng số proton trong hạt nhân.
- Tên nguyên tố hóa học: Mỗi nguyên tố hoá học đều có tên gọi riêng.
- Kí hiệu hóa học: được biểu diễn bằng một hoặc hai chữ cái trong tên nguyên tố.
Ôn tập nội dung kiến thức Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hoá học
- Nguyên tắc sắp xếp các nguyên tố hóa học trong bảng tuần hoàn
- Cấu tạo bảng tuần hoàn:
+ Ô nguyên tố
+ Chu kì
+ Nhóm
- Vị trí của các nguyên tố kim loại, phi kim và khí hiếm trong bảng tuần hoàn
- Ý nghĩa của bảng tuần hoàn:
+ Sử dụng bảng tuần hoàn để biết các thông tin của một nguyên tố hoá học
+ Sử dụng bảng tuần hoàn để biết vị trí của nguyên tố hoá học (ô, chu kì, nhóm)
Bài 1: Biết nguyên tử X có điện tích hạt nhân là +12, có 3 lớp electron, lớp ngoài cùng có 2 electron. Hãy xác định vị trí của X trong bảng tuần hoàn và tính chất hoá học cơ bản của nó.
Hướng dẫn giải
Vì điện tích hạt nhân là +12 nên số thứ tự của nguyên tố là 12 (ô số 12).
+ Có 3 lớp electron
=> Thuộc chu kì 3 của bảng tuần hoàn.
+ Có 2 electron lớp ngoài cùng
=> Thuộc nhóm II trong bảng tuần hoàn.
Dựa vào bảng tuần hoàn các nguyên tố hoá học xác định được:
+ Tên nguyên tố: magnesium.
+ Kí hiệu hoá học: Mg.
+ Khối lượng nguyên tử: 24 amu
+ Tính chất hoá học cơ bản: kim loại.
Bài 2: Tổng số proton, neutron và electron của nguyên tử X là 46. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 14.
a) Tính số proton, số neutron, số electron của nguyên tử X.
b) Tính khối lượng nguyên tử X.
c) Cho biết nguyên tử X có bao nhiêu lớp electron và chỉ ra số electron trên mỗi lớp.
Hướng dẫn giải
a) Gọi số hạt proton, neutron và electron trong nguyên tử X lần lượt là p, n và e.
Nguyên tử trung hòa về điện nên e = p (1)
Tổng số proton, neutron và electron của nguyên tử X là 46 nên:
p + n + e = 46 (2)
Thay e = p vào (2) ta được 2p + n = 46 hay n = 46 – 2p (3)
Trong X số hạt mang điện nhiều hơn số hạt không mang điện là 14 nên:
(p + e) – n = 14 (4)
Thay e = p; n = 46 – 2p vào (4) ta được:
2p – (46 – 2p) = 14 ⇒ p = 15
Vậy n = 46 – 2.15 = 16.
Số hạt proton, electron và neutron của X lần lượt là 15, 15, 16.
b) Khối lượng nguyên tử X là: 15 . 1 + 16 . 1 = 31 (amu)
c) Nguyên tử X có 15 electron được sắp xếp vào 3 lớp.
- Lớp thứ nhất (gần hạt nhân nhất) có 2 electron.
- Lớp thứ hai có 8 electron.
- Lớp thứ ba (lớp ngoài cùng) có 5 electron.
Học xong bài học này, em có thể:
- Hệ thống hóa các kiến thức đã học về nguyên tử, nguyên tố hóa học, bảng tuần hoàn các nguyên tố hóa học.
- Vận dụng được các kiến thức để giải một số dạng bài tập.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Khoa học tự nhiên 7 Cánh diều Bài tập (Chủ đề 1,2) cực hay có đáp án và lời giải chi tiết.
Các hạt cấu tạo nên hầu hết các nguyên tử là
Tại sao các nguyên tử trung hòa về điện?
Trong nguyên tử, số hạt proton và electron luôn bằng nhau.
Trong nguyên tử, số hạt neutron và proton luôn bằng nhau.
Trong nguyên tử, số hạt electron và neutron luôn bằng nhau.
Trong nguyên tử, số hạt negatron và electron luôn bằng nhau.
Nguyên tử sodium có 11 proton và 12 neutron. Khối lượng nguyên tử của sodium là
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Khoa học tự nhiên 7 Cánh diều Bài tập (Chủ đề 1,2)để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Giải bài 1 trang 26 SGK Khoa học tự nhiên 7 Cánh diều - CD
Giải bài 2 trang 26 SGK Khoa học tự nhiên 7 Cánh diều - CD
Giải bài 3 trang 26 SGK Khoa học tự nhiên 7 Cánh diều - CD
Giải bài 4 trang 26 SGK Khoa học tự nhiên 7 Cánh diều - CD
Giải bài 5 trang 27 SGK Khoa học tự nhiên 7 Cánh diều - CD
Giải bài 6 trang 27 SGK Khoa học tự nhiên 7 Cánh diều - CD
Giải bài 7 trang 27 SGK Khoa học tự nhiên 7 Cánh diều - CD
Giải bài 8 trang 27 SGK Khoa học tự nhiên 7 Cánh diều - CD
Giải bài 9 trang 27 SGK Khoa học tự nhiên 7 Cánh diều - CD
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Khoa học tự nhiên DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Các hạt cấu tạo nên hầu hết các nguyên tử là
Tại sao các nguyên tử trung hòa về điện?
Trong nguyên tử, số hạt proton và electron luôn bằng nhau.
Trong nguyên tử, số hạt neutron và proton luôn bằng nhau.
Trong nguyên tử, số hạt electron và neutron luôn bằng nhau.
Trong nguyên tử, số hạt negatron và electron luôn bằng nhau.
Nguyên tử sodium có 11 proton và 12 neutron. Khối lượng nguyên tử của sodium là
Cho các phát biểu sau:
(1) Trong mỗi nguyên tử, số hạt proton và electron luôn bằng nhau.
(2) Điện tích hạt nhân bằng tổng điện tích của các hạt proton trong nguyên tử.
(3) Khối lượng hạt nhân được coi là khối lượng nguyên tử.
(4) Proton và electron có khối lượng xấp xỉ bằng nhau.
Số phát biểu đúng là
Nguyên tố hóa học được đặc trưng bởi
Cho sơ đồ các nguyên tử X, Y, Z, T như sau:
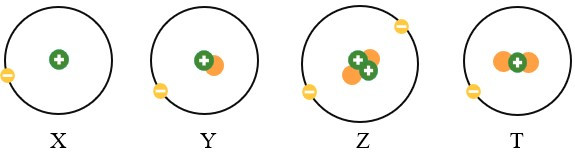
Các nguyên tử có tính chất hóa học giống nhau là
Cho các kí hiệu hóa học sau: H, Li, NA, O, Ne, AL, cA, K. Số kí hiệu hóa học viết sai là
Trong bảng tuần hoàn các nguyên tố hóa học được sắp xếp theo
Thứ tự tăng dần số hạt electron lớp ngoài cùng.
Bảng tuần hoàn gồm các nguyên tố hóa học mà vị trí được đặc trưng bởi
Biết nguyên tử của nguyên tố X có cấu tạo vỏ nguyên tử như sau: 11 electron, 3 lớp electron, lớp ngoài cùng có 1 electron. Phát biểu nào sau đây sai?
Những phát biểu sau nói về đặc điểm của các hạt cấu tạo nên nguyên tử. Với mỗi phát biểu, hãy điền tên hạt phù hợp vào ô trống.
| Phát biểu | Loại hạt |
| (1) Hạt mang điện tích dương | ? |
| (2) Hạt được tìm thấy cùng với proton trong hạt nhân | ? |
| (3) Hạt có thể xuất hiện với số lượng khác nhau trong các nguyên tử của cùng một nguyên tố. | ? |
| (4) Hạt có trong lớp vỏ xung quanh hạt nhân. | ? |
| (5) Hạt mang điện tích âm. | ? |
| (6) Hạt có khối lượng rất nhỏ, có thể bỏ qua khi tính khối lượng nguyên tử. | ? |
| (7) Hạt không mang điện tích | ? |
Điền thông tin thích hợp vào chỗ… trong mỗi câu sau:
a) Hạt nhân của nguyên tử được cấu tạo bởi các hạt…(?)…
b) Một nguyên tử có 17 proton trong hạt nhân, số electron chuyển động quanh hạt nhân là…(?)…
c) Một nguyên tử có 10 electron, số proton trong hạt nhân của nguyên tử đó là…(?)…
d) Khối lượng nguyên tử nguyên tố X bằng 19 amu, số electron của nguyên tử đó là 9. Số neutron của nguyên tử X là…(?)…
e) Một nguyên tử có 3 proton, 4 neutron và 3 electron. Khối lượng của nguyên tử đó là…(?)…
Viết kí hiệu hóa học của các nguyên tố sau: hydrogen, helium, carbon, nitrogen, oxygen, sodium.
Mô hình sắp xếp electron trong nguyên tử của nguyên tố X như sau:

a) Trong nguyên tử X có bao nhiêu electron và được sắp xếp thành mấy lớp?
b) Hãy cho biết tên nguyên tố X
c) Gọi tên một nguyên tố khác mà nguyên tử của nó có cùng số lớp electron với nguyên tử nguyên tố X
Hoàn thành những thông tin còn thiếu trong bảng sau:
| Tên nguyên tố | Kí hiệu hóa học | Nguyên tử của nguyên tố | |||
| Số proton | Số neutron | Số electron | Khối lượng nguyên tử (amu) | ||
| ? | ? | ? | 10 | 9 | ? |
| Sulfur | ? | ? | ? | 16 | 32 |
| ? | ? | 12 | ? | ? | 24 |
| ? | ? | 1 | ? | ? | 2 |
| ? | ? | ? | ? | 11 | 23 |
Số proton và số neutron của hai nguyên tử X và Y được cho trong bảng sau:
| Nguyên tử | X | Y |
| Số proton | 6 | 6 |
| Số neutron | 6 | 8 |
a) Tính khối lượng của nguyên tử X và nguyên tử Y
b) Nguyên tử X và nguyên tử Y có thuộc cùng một nguyên tố hóa học không? Vì sao?
Cho các nguyên tố sau: Ca, S, Na, Mg, F, Ne. Sử dụng bảng tuần hoàn các nguyên tố hóa học:
a) Hãy sắp xếp các nguyên tố trên theo chiều tăng dần điện tích hạt nhân
b) Cho biết mỗi nguyên tố trong dãy trên là kim loại, phi kim hay khí hiếm
Dựa vào bảng tuần hoàn, hãy cho biết một số thông tin của các nguyên tố có số hiệu nguyên tử lần lượt là 12, 15, 18. Điền các thông tin theo mẫu bảng sau:
| Số hiệu nguyên tử | Tên nguyên tố | Kí hiệu hóa học | Khối lượng nguyên tử | Chu kì | Nhóm | Kim loại, phi kim hay khí hiếm |
| 12 | ? | ? | ? | ? | ? | ? |
| 15 | ? | ? | ? | ? | ? | ? |
| 18 | ? | ? | ? | ? | ? | ? |
Biết nguyên tử của nguyên tố M có 3 lớp electron và có 2 electron ở lớp ngoài cùng. Hãy xác định vị trí của M trong bảng tuần hoàn (ô, chu kì, nhóm) và cho biết M là kim loại, phi kim hay khí hiếm.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *