Khi nghiên cứu quy luật biến đổi tính chất của các nguyên tố, các nhà khoa học đã tìm cách sắp xếp các nguyên tố vào một bảng theo nguyên tắc nhất định, gọi là bảng tuần hoàn các nguyên tố hóa học. Nội dung bài học Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hóa học sẽ tóm tắt nội dung cơ bản trong sách giáo khoa chương trình Khoa học tự nhiên lớp 7 SGK Cánh diều. Hi vọng tài liệu này sẽ hỗ trợ cho việc dạy và học của quý thầy cô và các em học sinh trở nên hiệu quả hơn. Mời thầy cô và các em cùng tham khảo chi tiết tại đây nhé!
- Nguyên tắt sắp xếp các nguyên tố trong bảng tuần hoàn:
+ Các nguyên tố hoá học được xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
+ Các nguyên tố được xếp trong cùng một hàng có cùng số lớp electron trong nguyên tử.
+ Các nguyên tố trong cùng một cột có tính chất hoá học tương tự nhau.

Bảng tuần hoàn gồm các ô được sắp xếp thành các hàng và các cột.
- Mỗi nguyên tố hoá học được xếp vào một ô của bảng tuần hoàn, gọi là ô nguyên tố.
Hình 3.1. Ô nguyên tố carbon
- Ô nguyên tố cho biết: số hiệu nguyên tử, kí hiệu hoá học, tên nguyên tố và khối lượng nguyên tử của nguyên tố đó.
Số hiệu nguyên tử (kí hiệu là Z) = số đơn vị điện tích hạt nhân = số proton = số electron trong nguyên tử của nguyên tố
- Chu kì gồm các nguyên tố mà nguyên tử của chúng có cùng số lớp electron và được xếp thành hàng theo chiều tăng dần của điện tích hạt nhân.
Số thứ tự của chu kì = số lớp electron trong nguyên tử của các nguyên tố
- Bảng tuần hoàn hiện nay gồm 7 chu kì, được đánh số từ 1 đến 7.
- Trong một chu kì, khi đi từ trái sang phải theo chiều tăng dần của điện tích hạt nhân:
+ Mở đầu chu kì là một kim loại điển hình (trừ chu kì 1)
+ Cuối chu kì là một phi kim điển hình (trừ chu kì 7)
+ Kết thúc chu kì là một khí hiếm.
Ví dụ: Trong chu kì 3, mở đầu chu kì là nguyên tố sodium (Na), là một kim loại điển hình, cuối chu kì là nguyên tố chlorine (Cl), là một phi kim điển hình và kết thúc chu kì là nguyên tố khí hiếm argon (Ar).
- Chu kì 1 gồm 2 nguyên tố là H và He. Nguyên tử của các nguyên tố này có 1 lớp electron. Điện tích hạt nhân tăng từ H là +1 đến He là +2.
Hình 3.2. Mô hình cấu tạo nguyên tử hydrogen và helium
- Chu kì 2 gồm 8 nguyên tố từ Li đến Ne. Nguyên tử của các nguyên tố này có 2 lớp electron. Điện tích hạt nhân tăng dần từ Li là +3 đến Ne là +10.
Hình 3.3. Mô hình cấu tạo nguyên tử lithium và neon
- Chu kì 3 gồm 8 nguyên tố từ Na đến Ar. Nguyên tử của các nguyên tố này có 3 lớp electron. Điện tích hạt nhân tăng dần từ Na là +11 đến Ar là +18.
Hình 3.4. Mô hình cấu tạo nguyên tử sodium và argon
- Nhóm gồm các nguyên tố có tính chất hoá học tương tự nhau, được xếp thành cột theo chiều tăng dần của điện tích hạt nhân.
- Bảng tuần hoàn gồm 18 cột:
+ 8 cột là nhóm A.
+ 10 cột là nhóm B (còn gọi là nhóm các nguyên tố kim loại chuyển tiếp).
- Nhóm A được đánh số thứ tự bằng số La Mã lần lượt từ nhóm IA đến VIIIA.
Số thứ tự của nhóm A = số electron lớp ngoài cùng trong nguyên tử của nguyên tố thuộc nhóm đó
+ Nhóm IA gồm các nguyên tố kim loại hoạt động mạnh (kim loại điển hình), trừ hydrogen (H). Nguyên tử của chúng đều có 1 electron ở lớp ngoài cùng. Điện tích hạt nhân của các nguyên tử kim loại trong nhóm IA tăng dần từ Li (+3) đến Fr (487).
+ Nhóm VIIA gồm các nguyên tố phi kim hoạt động mạnh (phi kim điển hình), trừ tennessine (Ts). Nguyên tử của chúng đều có 7 electron ở lớp ngoài cùng. Điện tích hạt nhân của các nguyên tử phi kim trong nhóm VIIA tăng dần từ F (49) đến At (+85).
+ Nhóm VIIIA gồm các nguyên tố khí hiếm. Nguyên tử của chúng đều có 8 electron ở lớp ngoài cùng (trừ helium). Điện tích hạt nhân tăng dần từ He (+2) đến Og (+118).
Hình 3.6. Nhóm IA và VIIA trong bảng tuần hoàn
Các nguyên tố hoá học được chia thành ba loại: kim loại, phi kim và khí hiếm.
Hình 3.7. Vị trí của các nguyên tố kim loại, phi kim, khí hiếm trong bảng tuần hoàn
Các nguyên tố kim loại
- Hơn 80% các nguyên tố trong bảng tuần hoàn là kim loại.
- Vị trí: ở phía bên trái và góc dưới bên phải của bảng tuần hoàn.
- Các nguyên tố nhóm IA (trừ hydrogen) đều là kim loại điển hình.
Các nguyên tố phi kim
- Vị trí: ở phía trên, bên phải của bảng tuần hoàn (các phi kim hoạt động mạnh nằm ở phía trên).
- Các nguyên tố nhóm VIIA hầu hết là những phi kim điển hình, fluorine ở đầu nhóm là phi kim hoạt động mạnh nhất.
Các nguyên tố khí hiếm
- Vị trí: Tất cả các nguyên tố nằm trong nhóm VIIIA
- Sử dụng bảng tuần hoàn để biết các thông tin của một nguyên tố hoá học: tên nguyên tố, số hiệu nguyên tử, kí hiệu hoá học, khối lượng nguyên tử.
- Sử dụng bảng tuần hoàn để biết vị trí của nguyên tố hoá học (ô, chu kì, nhóm). Từ đó nhận ra được nguyên tố kim loại, phi kim hay khí hiếm.
+ Các nguyên tố ở nhóm IA, IIA, IIIA là kim loại (trừ hydrogen và boron).
+ Hầu hết các nguyên tố ở nhóm VA, VIA, VIIA là phi kim.
+ Các nguyên tố ở nhóm VIIIA là khí hiếm.
Ví dụ: Sử dụng bảng tuần hoàn biết được nguyên tố sulfur (S) ở ô số 16, chu kì 3, nhóm VIA và đó là nguyên tố phi kim.
|
1. Nguyên tắc sắp xếp các nguyên tố hoá học trong bảng tuần hoàn: Các nguyên tố được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử. Các nguyên tố cùng chu kì có cùng số lớp electron. Các nguyên tố cùng nhóm có tính chất hoá học tương tự nhau. 2. Bảng tuần hoàn gồm các nguyên tố hoá học mà vị trí được đặc trưng bởi ô nguyên tố, chu kì và nhóm. Số hiệu nguyên tử (kí hiệu là Z) = số đơn vị điện tích hạt nhân = số proton = số electron trong nguyên tử của nguyên tố Số thứ tự của chu kì = số lớp electron trong nguyên tử của các nguyên tố Số thứ tự của nhóm A = số electron lớp ngoài cùng trong nguyên tử của nguyên tố 3. Bảng tuần hoàn cho biết: các thông tin của một nguyên tố; vị trí của các nguyên tố; nguyên tố đó là kim loại, phi kim hay khí hiếm.
|
Bài 1: Quan sát mô hình cấu tạo của bốn nguyên tử thuộc bốn nguyên tố có kí hiệu lần lượt là A1, A2, A3, A4 dưới đây:
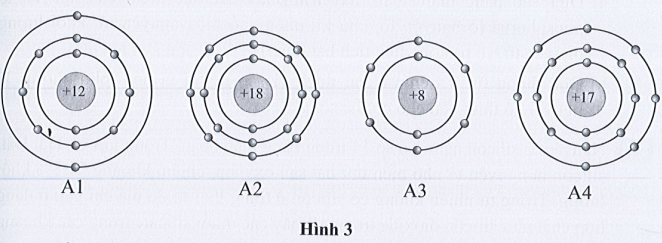
Điền các thông tin còn thiếu vào bảng sau đây:
| Nguyên tử nguyên tố | A1 | A2 | A3 | A4 |
| Số lớp electron |
|
|
|
|
| Số electron lớp ngoài cùng |
|
|
|
|
| Số hiệu nguyên tử |
|
|
|
|
| Số proton |
|
|
|
|
Hướng dẫn giải
Trong nguyên tử: số hiệu nguyên tử = số proton = số electron
| Nguyên tử nguyên tố | A1 | A2 | A3 | A4 |
| Số lớp electron | 3 | 3 | 2 | 3 |
| Số electron lớp ngoài cùng | 2 | 8 | 6 | 7 |
| Số hiệu nguyên tử | 12 | 18 | 8 | 17 |
| Số proton | 12 | 18 | 8 | 17 |
Bài 2: Quan sát bảng tuần hoàn, ô nguyên tố số 11 và cho biết:
a) Tên nguyên tố, kí hiệu nguyên tố hóa học, khối lượng nguyên tử, số hiệu nguyên tử
b) Số proton, số electron và số lớp electron
c) Những nguyên tố nào trong bảng tuần hoàn có tính chất hóa học tương tự nguyên tố trên
Hướng dẫn giải
a) Ô nguyên tố số 11 là nguyên tố sodium (Na), khối lượng nguyên tử bằng 23, số hiệu nguyên tử bằng 11
b) Số hiệu nguyên tử = số proton = số electron = 11
Số lớp electron = số thứ tự chu kì = 3
Nguyên tố sodium (Na) có 11 proton trong hạt nhân, 11 electron và có 3 lớp electron trong nguyên tử
c) Những nguyên tố kim loại thuộc nhóm IA có tính chất tương tự nguyên tố Na (vì nguyên tố Na là nguyên tố kim loại thuộc nhóm IA): Li, K, Rb, Cs, Fr
Học xong bài học này, em có thể:
- Nêu được các nguyên tắc xây dựng bảng tuần hoàn các nguyên tố hoá học.
- Mô tả được cấu tạo bảng tuần hoàn gồm ô, nhóm, chu kì.
- Sử dụng được bảng tuần hoàn để chỉ ra các nhóm nguyên tố kim loại, phi kim, khí hiếm.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Khoa học tự nhiên 7 Cánh diều Chủ đề 2 Bài 3 cực hay có đáp án và lời giải chi tiết.
Thông tin trên ô nguyên tố trong bảng tuần hoàn cho biết
số hiệu nguyên tử, kí hiệu hóa học, tên nguyên tố và số lớp electron của nguyên tố đó.
số hiệu nguyên tử, kí hiệu hóa học, tên nguyên tố và khối lượng nguyên tử của nguyên tố đó.
Cho biết các nguyên tử của nguyên tố M có 3 lớp electron và có 1 electron ở lớp ngoài cùng. Nguyên tố M có vị trí trong bảng tuần hoàn như sau
Các nguyên tố trong bảng tuần hoàn các nguyên tố hoá học được sắp xếp theo thứ tự tăng dẫn của
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Khoa học tự nhiên 7 Cánh diều Chủ đề 2 Bài 3để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Mở đầu trang 19 SGK Khoa học tự nhiên 7 Cánh diều - CD
Câu hỏi 1 trang 20 SGK Khoa học tự nhiên 7 Cánh diều - CD
Câu hỏi 2 trang 20 SGK Khoa học tự nhiên 7 Cánh diều - CD
Tìm hiểu thêm trang 20 SGK Khoa học tự nhiên 7 Cánh diều - CD
Luyện tập 1 trang 20 SGK Khoa học tự nhiên 7 Cánh diều - CD
Luyện tập 2 trang 21 SGK Khoa học tự nhiên 7 Cánh diều - CD
Luyện tập 3 trang 21 SGK Khoa học tự nhiên 7 Cánh diều - CD
Câu hỏi 3 trang 21 SGK Khoa học tự nhiên 7 Cánh diều - CD
Câu hỏi 4 trang 22 SGK Khoa học tự nhiên 7 Cánh diều - CD
Luyện tập 4 trang 22 SGK Khoa học tự nhiên 7 Cánh diều - CD
Luyện tập 5 trang 23 SGK Khoa học tự nhiên 7 Cánh diều - CD
Câu hỏi 5 trang 23 SGK Khoa học tự nhiên 7 Cánh diều - CD
Luyện tập 6 trang 24 SGK Khoa học tự nhiên 7 Cánh diều - CD
Vận dụng trang 24 SGK Khoa học tự nhiên 7 Cánh diều - CD
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Khoa học tự nhiên DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Thông tin trên ô nguyên tố trong bảng tuần hoàn cho biết
số hiệu nguyên tử, kí hiệu hóa học, tên nguyên tố và số lớp electron của nguyên tố đó.
số hiệu nguyên tử, kí hiệu hóa học, tên nguyên tố và khối lượng nguyên tử của nguyên tố đó.
Cho biết các nguyên tử của nguyên tố M có 3 lớp electron và có 1 electron ở lớp ngoài cùng. Nguyên tố M có vị trí trong bảng tuần hoàn như sau
Các nguyên tố trong bảng tuần hoàn các nguyên tố hoá học được sắp xếp theo thứ tự tăng dẫn của
Số hiệu nguyên tử của một nguyên tố là
Bảng tuần hoàn các nguyên tố hoá học được cấu tạo từ
Phát biểu nào sau đây không đúng?
Số thứ tự của chu kì bằng số electron ở lớp ngoài cùng của nguyên tử các nguyên tố thuộc chu kì đó.
Số thứ tự của chu kì bằng số lớp electron của nguyên tử các nguyên tố thuộc chu kì đó.
Các nguyên tố trong cùng chu kì được sắp xếp theo chiều điện tích hạt nhân tăng dần.a
Phát biểu nào sau đây là đúng?
Các nguyên tố kim loại tập trung hầu hết ở góc trên bên phải của bảng tuần hoàn.
Các nguyên tố kim loại tập trung hầu hết ở góc dưới bên trái của bảng tuần hoàn.
Các kim loại kiềm trong nhóm IA đều có số electron lớp ngoài cùng là bao nhiêu?
Những nguyên tố nào sau đây thuộc nhóm VIIA (Halogen)?
Cho biết một nguyên tử của nguyên tố X có điện tích hạt nhân là +17. Hãy chọn câu đúng trong các câu sau:
Nguyên tố X ở chu kì 3, nhóm VIIA; là phi kim; có 17 proton, 7 electron.
Nguyên tố X ở chu kì 3, nhóm VIIA; là phi kim; có 17 proton, 17 electron.
Nguyên tố X ở chu kì 2, nhóm VIIA; là kim loại; có 17 proton, 17 electron.
Nguyên tố X ở chu kì 2, nhóm VIIA; là phi kim; có 17 proton, 7 electron.
Ai nhanh hơn?
Hãy sắp xếp những tấm thẻ vào các ô trong bảng dưới đây theo quy luật nhất định. Hãy cho biết các tấm thẻ được sắp xếp theo quy luật nào theo hàng và theo cột.
Tương tự như vậy, có thể sắp xếp các nguyên tố hóa học theo quy luật vào một bảng được không?
Cho biết điện tích hạt nhân của mỗi nguyên tử C, Si, O, P, N, S lần lượt là 6, 14, 8, 15, 7, 16. Hãy sắp xếp các nguyên tố trên theo chiều điện tích hạt nhân tăng dần từ trái sang phải và từ trên xuống dưới
| C | ? | O |
| Si | ? | ? |
Hình 3.1 cho biết các thông tin gì về nguyên tố carbon?
Hình 3.1. Ô nguyên tố carbon
Việc tìm ra bảng tuần hoàn là một trong những phát hiện xuất sắc nhất trong ngành hóa học. Em hãy tìm hiểu lịch sử phát minh ra bảng tuần hoàn các nguyên tố hóa học
Hãy tìm nguyên tố hóa học có số thứ tự lần lượt là 16 và 20 trong bảng tuần hoàn. Đọc tên hai nguyên tố. Hãy cho biết số hiệu nguyên tử, kí hiệu hóa học và khối lượng nguyên tử của hai nguyên tố đó.
Nguyên tố X có số thứ tự 15 trong bảng tuần hoàn. Hãy cho biết nguyên tố đó ở chu kì nào và có mấy lớp electron
Dựa vào hình 3.4, hãy cho biết một số thông tin về nguyên tố natri và argon (số hiệu nguyên tử, điện tích hạt nhân, số lớp electron, chu kì, số electron ở lớp ngoài cùng)
Hình 3.4. Mô hình cấu tạo nguyên tử sodium và argon
Quan sát bảng tuần hoàn, cho biết số hiệu nguyên tử, số lớp electron lần lượt của nguyên tử carbon (C) và nhôm (Al). Hai nguyên tố đó nằm ở chu kì nào trong bảng tuần hoàn?
Quan sát hình 3.5 và bảng tuần hoàn, hãy cho biết số electron lớp ngoài cùng của nguyên tử Li (lithium) và Cl (chlorine). Hai nguyên tố đó nằm ở nhóm nào trong bảng tuần hoàn
Nguyên tố X tạo nên chất khí duy trì sự hô hấp của con người và có nhiều trong không khí. Hãy cho biết tên của nguyên tố X. Nguyên tố X nằm ở ô nào và chu kì nào trong bảng tuần hoàn
Cho các nguyên tố có số thứ tự lần lượt là 9, 18 và 19. Số electron lớp ngoài cùng của mỗi nguyên tố trên là bao nhiêu? Cho biết mỗi nguyên tố nằm ở nhóm nào và đó là kim loại, phi kim hay khí hiếm
Quan sát bảng tuần hoàn các nguyên tố hóa học, hãy cho biết vị trí của các nguyên tố kim loại, phi kim và khí hiếm

Nguyên tố X nằm ở chu kì 2, nhóm VA trong bảng tuần hoàn. Hãy cho biết một số thông tin của nguyên tố X (tên nguyên tố, kí hiệu hóa học, khối lượng nguyên tử), vị trí ô của nguyên tố trong bảng tuần hoàn. Nguyên tố đó là kim loại, phi kim hay khí hiếm?
Hãy tự thiết kế bảng tuần hoàn với 3 chu kì và 8 nhóm bằng các tấm thẻ (bìa) cho 18 nguyên tố có số thứ tự từ 1 đến 18 với các thông tin mà em biết. Tô màu để phân biệt các nguyên tố kim loại, phi kim, khí hiếm
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *