Qua nội dung bài giảng Bài 23: Ôn tập chương 7 môn Hóa học 10 chương trình Kết nối tri thức được DapAnHay biên soạn và tổng hợp giới thiệu đến các em học sinh, giúp các em tổng hợp kiến thức về nguyên tố nhóm Halogen cũng như các tính chất và ứng dụng của nó.... Để đi sâu vào tìm hiểu và nghiên cứu nội dung bài học, mời các em cùng tham khảo nội dung chi tiết trong bài giảng sau đây.
- Nhóm halogen gồm: Flo (F), Clo (Cl), Brom (Br), Iot (I), Atatin (At) (Atatin không gặp trong tự nhiên, nó được điều chế nhân tạo trong các lò phản ứng hạt nhân nên được xem xét chủ yếu trong nhóm các nguyên tố phóng xạ).
- Các nguyên tố halogen thuộc nhóm VIIA. Chúng đứng gần cuối chu kì, ngay trước các nguyên tố khí hiếm.
- Nguyên tử các nguyên tố halogen đều có 7e lớp ngoài cùng (ns2 np5)
- Ở trạng thái tự do, 2 nguyên tử halogen góp chung 1e với nhau tạo 1 liên kết cộng hóa trị không cực.
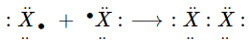
(X là kí hiệu chỉ các nguyên tố halogen)
⟶ Công thức cấu tạo: X−X
⟶ Công thức phân tử: X2
- Liên kết trong phân tử X2 không bền lắm, dễ bị tách thành 2 nguyên tử X.
- Trong phản ứng hóa học, các nguyên tử X dễ thu thêm 1e.
⟹ Tính chất hóa học cơ bản của các halogen là tính oxi hóa mạnh.
a. Sự biến đổi tính chất vật lí của các đơn chất
Từ F đến I ta thấy:
- Trạng thái tập hợp: khí ⟶ lỏng ⟶ rắn.
- Màu sắc: đậm dần.
- Nhiệt độ nóng chảy, nhiệt độ sôi tăng dẫn
b. Sự biến đổi độ âm điện
- Độ âm điện tương đối lớn.
- Giảm dần từ F đến I.
- Trong hợp chất:
+ F có độ âm điện lớn nhất nên chỉ có số oxi hóa −1.
+ Các nguyên tố halogen khác, ngoài số oxi hóa −1 còn có các số oxi hóa +1, +3, +5, +7.
c. Sự biến đổi tính chất hóa học của các đơn chất
- Các đơn chất halogen giống nhau về tính chất hóa học cũng như thành phần và tính chất của các hợp chất do chúng tạo thành (Do lớp e ngoài cùng có cấu hình tương tự nhau ( ns2np5) .
- Halogen là những phi kim điển hình. Tính oxi hóa giảm dần từ Flo đến Iot.
- Các đơn chất halogen oxi hóa được:
+ Hầu hết các kim loại ⟶ muối halogenua.
+ H2 ⟶ hợp chất khí không màu hiđro halogenua (khí này tan trong nước tạo dung dịch axit halogenhiđric).
- HCl, HBr, HI tác dụng với kim loại tạo muối và khí H2 : 2xHX + M → MClx + xH2
- HCl, HBr, HI không tác dụng được với Cu, Ag, Au, Pt.
- HCl, HBr, HI khi tác dụng với Fe và Cr chỉ tạo thành Fe2+ và Cr2+.
→ Tính acid tăng dần từ HF (acid yếu) đến HI (acid rất mạnh)
- Hầu hết các muối halide đều dễ tan trong nước, trừ một số muối không tan như silver chloride, silver bromide, silver iodide và một số muối ít tan như lead chroride, lead bromide.
- lon halide, muối halide: Tính khử tăng dần từ fluoride đến iodide.
Bài 1: Trong phương trình MnO2 + HCl → MnCl2 + Cl2 + H2O thì hệ số cân bằng của HCl là bao nhiêu?
A. 1.
B. 2 .
C. 3.
D. 4.
Hướng dẫn giải
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
Đáp án D
Bài 2: Những hiđro halogenua có thể thu được khi cho H2SO4 đặc lần lượt tác dụng với các muối NaF, NaCl, NaBr, NaI là
A. HF, HCl, HBr, HI
B. HF, HCl, HBr và một phần HI
C. HF, HCl, HBr
D. HF, HCl
Hướng dẫn giải
2NaF + H2SO4 → Na2SO4 + 2HF
2NaCl + H2SO4 → Na2SO4 + 2HCl
2NaBr + 2H2SO4 → Na2SO4 + Br2 + SO2 + 2H2O
8NaI + 5H2SO4 → 4Na2SO4 + 4I2 + H2S + 4H2O
Đáp án D
Bài 3: Trình bày phương pháp hóa học nhận biết các dung dịch sau: NaNO3 , NaOH, Na2SO4 , NaCl, HCl, H2SO4
Hướng dẫn giải
Trích mỗi dung dịch một ít làm mẫu thử:
Cho quì tím lần lượt vào các mẫu thử trên:
- Mẫu thử làm quì tím hóa xanh là dung dịch NaOH
- Mẫu thử làm quì tím hóa đỏ là dung dịch HCl và H2SO4 (nhóm 1)
- Mẫu thử không làm đổi màu quì tím là NaNO3, Na2SO4 , NaCl (nhóm 2)
Cho dung dịch BaCl2 hoặc dung dịch Ba(NO3)2 hoặc dung dịch Ba(OH) 2 hoặc BaO lần lượt vào hai chất ở nhóm 1
- Mẫu thử tạo kết tủa trắng là H2SO4
BaCl2 + H2SO4 → BaSO4 ↓ + 2HCl
- Còn lại là dung dịch HCl
Cho dung dịch BaCl2 hoặc dung dịch Ba(NO3)2 hoặc dung dịch Ba(OH) 2 lần lượt vào hai chất ở nhóm 2.
- Mẫu thử nào tọa kết tủa trắng là Na2SO4
BaCl2 + H2SO4 → BaSO4 ↓ + 2HCl
- Hai mẫu thử còn lại không có hiện tượng gì
Cho dung dịch AgNO3 lần lượt vào hai mẫu thử còn lại. Mẫu thử nào kết tủa trắng là NaCl, còn lại là NaNO3
AgNO3 + NaCl → AgCl↓ + NaNO3
Sau bài học này, học sinh có thể:
- Biết cách phân biệt các ion F-, Cl-, Br-,I-.
- Trình bày được tính khử của các ion halide (Cl-, Br-,I-) thông qua phản ứng với chất oxi hoá là sulfuric add đặc
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 10 KNTT Bài 23 cực hay có đáp án và lời giải chi tiết.
Cho 5,6 gam một oxit kim loại tác dụng vừa đủ với HCl cho 11,1 gam muối clorua của kim loại đó. Cho biết công thức oxit kim loại?
Tổng hệ số cân bằng (là các số nguyên, tối giản) của phương trình: KMnO4 + HCl → … là:
Nhận định nào sau đây là không chính xác về HCl:
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 10 KNTT Bài 23để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Giải bài 1 trang 118 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải bài 2 trang 118 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải bài 3 trang 118 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải bài 4 trang 118 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải bài 5 trang 118 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải bài 6 trang 118 SGK Hóa học 10 Kết nối tri thức - KNTT
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Cho 5,6 gam một oxit kim loại tác dụng vừa đủ với HCl cho 11,1 gam muối clorua của kim loại đó. Cho biết công thức oxit kim loại?
Tổng hệ số cân bằng (là các số nguyên, tối giản) của phương trình: KMnO4 + HCl → … là:
Nhận định nào sau đây là không chính xác về HCl:
Chất có tính axit mạnh nhất trong cách axit sau là:
Đổ dung dịch AgNO3 lần lượt vào 4 dung dịch: NaF, NaCl, NaBr và NaI thì thấy:
Ion Ca2+ có cấu hình electron giống với cấu hình electron của nguyên tử khí hiếm và ion halogen nào sau đây?
Tìm tỉ lệ a : b thõa mãn những ý sau đây nung X gồm a mol Fe và b mol S trong khí trơ, với %H = 50%, thu được hỗn hợp rắn Y. Cho Y vào HCl dư, sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Z có tỉ khối so với H2 bằng 5.
Trong 5,6 gam Fe với 2,4 gam S được hỗn hợp rắn M, nếu cho M vào HCl, giải phóng hỗn hợp khí X và còn lại một phần không tan G. Để đốt cháy hoàn toàn X và G cần vừa đủ bao nhiêu lít khí O2(đktc)?
39,5 gam hỗn hợp X gồm MgCO3, MgCl2, BaCO3 tác dụng vừa đủ với dung dịch HCl thu được dung dịch chứa 41,7 gam chất tan. Phần trăm khối lượng nguyên tố oxi trong hỗn hợp X là
Đặc điểm chung của halogen?
Liên kết trong phân tử nào sau đây có độ phân cực lớn nhất?
A. H-F
B. H-Cl
C. H-Br
D. H-I
Trong nhóm halogen, từ F đến I, bán kính nguyên tử biến đổi theo chiều nào?
A. Giảm dần
B. Không đổi
C. Tăng dần
D. Tuần hoàn
Trong dãy đơn chất từ F2 đến I2, chất có tính oxi hóa mạnh nhất là
A. F2
B. Cl2
C. Br2
D. I2
Khi tiến hành điều chế và thu khí Cl2 vào bình, để ngăn khí Cl2 thoát ra ngoài gây độc, cần đậy miệng bình thu khí Cl2 bằng bông có tẩm dung dịch
A. NaCl
B. HCl
C. NaOH
D. KCl
Làm muối là nghề phổ biến tại nhiều vùng ven biển Việt Nam. Một hộ gia đình tiến hành làm muối trên ruộng muối chứa 200 000 L nước biển. Giả thiết 1 L biển có chứa 30 g NaCl và hiệu suất quá trình làm muối thành phẩm đạt 60%
Khối lượng muối hộ gia đình thu được là
A. 1 200 kg
B. 10 000 kg
C. 6 000 kg
D. 3 600 kg
Cho X, Y là hai nguyên tố halogen có trong tự nhiên, ở hai chu kì liên tiếp, ZX < ZY. Hòa tan hoàn toàn 0,402 g hỗn hợp NaX và NaY vào nước, thu được dung dịch E. Cho từ từ E vào cốc đựng dung dịch AgNO3 dư, thu được 0,574 g kết tủa.
Kí hiệu của nguyên tố X và Y lần lượt là
A. F và Cl
B. Cl và Br
C. Br và I
D. Cl và I
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *