Mời các em học sinh cùng tham khảo nội dung bài học Bài 15: Phản ứng oxi hóa - khử môn Hóa 10 chương trình SGK Kết nối tri thức được đội ngũ DapAnHay biên soạn và tổng hợp bên dưới đây để nắm được các khái niệm về số oxh, các phản ứng, cách mô tả củng như giải thành thạo một số bài toán liên quan.
a. Khái niệm
- Số oxi hoá là điện tích quy ước của nguyên tử trong phân từ khi coi tất cả các electron liên kết đều chuyện hoàn toàn về nguyên tử có độ âm điện lớn hơn.
- Số oxi hoá được viết ở dạng số đại số, dấu viết trước, số viết sau.
Ví dụ 1: Xét phân tử NaCl
Nguyên tử Na nhường 1 electron cho nguyên tử Cl, khi đó nguyên tử Na trở thành ion dương mang điện tích +1 (số oxi hoá của Na là +1) và nguyên tử Cl trở thành ion âm mang điện tích -1 (số oxi hoá của Cl là -1): \(\mathop {Na}\limits^{ + 1} \mathop {Cl}\limits^{ - 1} \)
Ví dụ 2: Xét phân tử H2O.
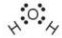
Độ âm điện của nguyên tử o lớn hơn độ âm điện của nguyên tử H, nếu các cặp electron liên kết chuyển hoàn toàn về nguyên tử O thì nguyên tử O có thêm 2 electron và trở thành ion âm có điện tích -2 (số oxi hoá của O là -2); mỗi nguyên tử H mất đi 1 electron và trở thành ion dương có điện tích +1 (số oxi hoá của H là +1): \(\mathop {{H_2}}\limits^{ + 1} \mathop O\limits^{ - 2} \)
Ví dụ 3: Xét phân tử H2
H : H
Hai nguyên tử H giống nhau nên cặp electron liên kết không lệch về nguyên tử nào.
Do vậy, mỗi nguyên tử H đều trung hoà điện, có điện tích bằng 0 và số oxi hoá là 0.
\(\mathop {{H_2}}\limits^0 \)
Số oxi hoá thường được dùng để lập phương trình hoá học của phản ứng oxi hoá - khử.
b. Quy tắc xác định số oxi hoá
Thông thường, số oxi hoá của nguyên tử được xác định trực tiếp từ công thức phân tử theo các quy tắc sau:
Quy tắc 1. Trong đơn chất, số oxi hoá của nguyên tử bằng 0
Ví dụ: \(\mathop C\limits^0 \,\,\,\,\,\,\mathop {Na}\limits^0 \,\,\,\,\,\mathop {{H_2}}\limits^0 \,\,\,\,\,\,\mathop {{O_2}}\limits^0 \)
Quy tắc 2. Trong phân tử các hợp chất, thông thường số oxi hoá của hydrogen là +1, của oxygen là -2, các kim loại điền hình có số oxi hoá dương bằng số electron hoá trị.
Bảng 15.1. Số oxi hoá thường gặp của một số nguyên tử trong hợp chất

Quy tắc 3. Trong hợp chất, tổng số oxi hoá của các nguyên tử trong phân tử bằng 0.
Ví dụ: \(\mathop {A{l_2}}\limits^{ + 3} \mathop {{O_3}}\limits^{ - 2} \)
Tổng số oxi hoá = (+3).2 + (-2).3 = 0
Quy tắc 4. Trong ion đơn nguyên tử, SỐ oxi hoá của nguyên tử bằng điện tích ion trong ion đa nguyên tử, tổng số oxi hoá của các nguyên tử bằng điện tích lon.
Ví dụ: \(\,{\left[ {\mathop N\limits^{ - 3} \mathop {{H_4}}\limits^{ + 1} } \right]^ + }\,\,\)
Tổng số oxi hoá = (-3) + (+1).4 = +1.
ÁP DỤNG: Sử dụng các quy tắc này có thể xác định số oxi hoá của một nguyên tử | trong hợp chất khi biết số oxi hoá của các nguyên tử còn lại.
Ví dụ: Xác định số oxi hoá của nguyên tử C trong phân tử CaCO3
Dựa vào Bảng 15. 1, biết được số oxi hoá của Ca là +2 và O là -2.
Số oxi hoá của từng nguyên tử: \(\mathop {Ca}\limits^{ + 2} \mathop C\limits^x \mathop {{O_3}}\limits^{ - 2} \)
Phân tử CaCO3 trung hoà điện nên tổng số oxi hoá của các nguyên tử bằng 0:
(+2) + x + (-2).3 = 0 nên x = +4.
|
|---|
a. Chất oxi hoá, chất khử
Ví dụ 1: Đưa mẫu thân gỗ nóng đỏ vào bình đựng khí O2, mẫu than cháy sáng.
\(\mathop C\limits^0 + \mathop {{O_2}}\limits^0 \to \mathop C\limits^{ + 4} \mathop {{O_2}}\limits^{ - 2} \)
Trong phản ứng trên, nguyên tử C nhường 4 electron, là chất khử, phân tử O, nhận 4 electron, là chất oxi hoá.
Co → C+4 + 4e (quá trình oxi hoá)
\(\mathop {{O_2}}\limits^0 \) + 4e → 2\(\mathop O\limits^{ - 2} \) (quá trình khử)
Ví dụ 2: Phản ứng đốt cháy methane.
\(\mathop C\limits^{ + 4} \mathop {{O_2}}\limits^{ - 2} \)
Chất oxi hoá là oxygen, chất khử là methane.
Ví dụ 3: Phản ứng khử FeO, bằng CO để sản xuất gang và thép.
\(\mathop {F{e_2}}\limits^{ + 3} \mathop {{O_3}}\limits^{} + 3\mathop {CO}\limits^0 \to 2\mathop {Fe}\limits^0 + 3\mathop C\limits^{ + 4} \mathop {{O_2}}\limits^{ - 2} \)
Chất oxi hoá là iron(III) oxide, chất khử là carbon monooxide
Chất khử là chất nhường electron, chất oxi hoá là chất nhận electron.
Quá trình oxi hoá là quá trình chất khử nhường electron, quá trình khử là quá trình chất Oxi hoá nhận electron.
b. Phản ứng oxi hoá - khử
- Phản ứng oxi hoá - khử là phản ứng hoá học xảy ra đồng thời quá trình nhường và quá trình nhận electron.
- Dấu hiệu để nhận biết phản ứng oxi hoá - khử là có sự thay đổi số oxi hoá của các nguyên tử.
| Bản chất của phản ứng oxi hoá - khử: - Phản ứng oxi hóa khử là phản ứng hóa học, trong đó có sự chuyển electron giữa các chất trong phản ứng hay phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của một số nguyên tố. + Quá trình oxh (sự oxh) là quá trình nhường electron. + Quá trình khử (sự khử) là quá trình thu electron. |
|---|
- Phương pháp thăng bằng electron được dùng để lập phương trình hoá học của phản ứng oxi hoá - khử theo nguyên tắc:
- Tổng số electron chất khử nhường bằng tổng số electron chất oxi hoá nhận.
Ví dụ: Quá trình Oswald (Ot-xvan) dùng để sản xuất nitric acid từ ammonia, được đề xuất vào năm 1902. Ở giai đoạn đầu của quá trình, ammonia bị oxi hoá bởi oxygen ở nhiệt độ cao khi có chất xúc tác: NH3 + O2 → NO + H2O
- Theo phương pháp thăng bằng electron, phương trình hoá học của phản ứng trên được lập theo các bước như sau:
+ Bước 1. Xác định các nguyên tử có sự thay đổi số oxi hoá, từ đó xác định chất oxi hoá, chất khử:
\(\mathop N\limits^{ - 3} \mathop {{H_3}}\limits^{} + \mathop {{O_2}}\limits^0 \to \mathop N\limits^{ + 2} \mathop O\limits^{ - 2} + \mathop H\limits^{} \mathop {_2O}\limits^{ - 2} \)
+ Bước 2. Biểu diễn quá trình oxi hoá, quá trình khử:
N-3 → N+2 + 5e
\(\mathop {{O_2}}\limits^0 \) + 4e → 2O-2
+ Bước 3. Tìm hệ số thích hợp cho chất khử và chất oxi hoá dựa trên nguyên tắc: Tổng số electron chất khử nhường bằng tổng số electron chất oxi hoá nhận.
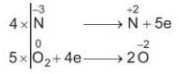
+ Bước 4. Đặt hệ số của chất oxi hoá và chất khử vào sơ đồ phản ứng, từ đó tính ra hệ số của các chất khác có mặt trong phương trình hoá học. Kiểm tra sự cân bằng số nguyên tử của các nguyên tố ở hai vế.
4NH3 + 5O2 → 4NO + 6H2O
| Nguyên tắc lập phương trình hoá học của phản ứng oxi hoá - khử theo phương pháp thăng bằng electron: \(\sum \) số electron chất khử nhường = \(\sum \) số electron chất oxi hoá nhận. |
|---|
Trong thực tiễn, phản ứng oxi hoá - khử rất phổ biến, dưới đây là một số trường hợp điển hình.
a. Sự cháy
- Phản ứng cháy là phản ứng oxi hoá - khử xảy ra ở nhiệt độ cao giữa chất cháy và chất Oxi hoá. Trong phản ứng cháy, chất cháy thường là nhiên liệu (than đá, khi thiên nhiên, xăng. dầu,...), còn chất oxi hoá thường là oxygen. Sự cháy kèm theo sự toả nhiệt và phát sáng, tạo ra nhiệt lượng đủ để duy trì sự cháy.
Ví dụ: Phản ứng oxi hoá - khử xảy ra khi đốt cháy carbon trong than đá và butane trong khí gas
C + O2 → CO2
2C4H10 + 13O2 → 8CO2 + 10H2O
b. Sự han gỉ kim loại
- Sau một thời gian sử dụng, nhiều thiết bị, máy móc, vật dụng bằng kim loại thường bị han gi do sự oxi hoá của oxygen trong không khí. Đặc biệt, nước ta có khí hậu nhiệt đới, độ ẩm cao nên sự han gỉ kim loại xảy ra rất phổ biến.
Ví dụ: Trong không khí ấm, các vật dụng bằng thép bị oxi hoá tạo gỉ sắt.
4Fe + 3O2 + xH2O → 2Fe2O3.xH2O
c. Sản xuất hoá chất
- Trong công nghiệp, phần lớn các phản ứng hoá học xảy ra trong các quy trình sản xuất là phản ứng oxi hoá - khử. Ví dụ: Sulfuric acid là hoá chất quan trọng trong công nghiệp, được sản xuất chủ yếu từ sulfur hoặc quặng pyrite.
- Sơ đồ phản ứng:
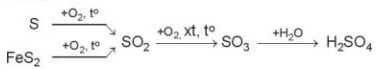
d. Chuyển hoá các chất trong tự nhiên
- Trong tự nhiên cũng xảy ra rất nhiều quá trình kèm theo phản ứng oxi hoá - khử.
Ví dụ:
Lúa chiêm lấp ló đầu bờ
Hễ nghe tiếng sấm phất cờ mà lên
(Ca dao Việt Nam)
- Đây là hiện tượng cây lúa phát triển nhanh khi có những cơn mưa rào đầu tiên kèm theo sấm sét vào khoảng cuối mùa xuân.
- Tia sét tạo ra tia lửa điện, là điều kiện cho nitrogen phản ứng với oxygen: N2 + O2 → 2NO
- Khí NO sinh ra nhanh chóng chuyền hoá thành NO2, sau đó tiếp tục bị oxi hoá thành HNO3:
2NO + O2 → 2NO2
4NO2 + O2 + 2H2O → 4HNO3
- Nitric acid tan vào nước mưa và chuyển hoá thành gốc nitrate (NO3-), cung cấp chất đạm cho cây lúa. Nhờ quá trình trên, hằng năm một lượng lớn phân đạm tự nhiên được bổ sung cho đất.
e. Xác định nồng độ một chất bằng phản ứng oxi hoá - khử
- Trong thực tế, dung dịch thuốc tím (KMnO4) được sử dụng phổ biến như một tác nhân oxi hoá mạnh để xác định hàm lượng các chất khử như iron(II), hydrogen peroxide, oxalic acid,...
Ví dụ: Trong quá trình bảo quản, một mẫu iron(II) sulfate bị oxi hoá một phần thành hợp chất tron(III). Hàm lượng tron(II) sulfate còn lại trong mẫu được xác định thông qua phản ứng với dung dịch thuốc tím có nồng độ đã biết:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
| Các phản ứng oxi hoá - khử xảy ra phổ biến trong thực tiễn: sự cháy, sự han gỉ của kim loại, sản xuất hoá chất, chuyển hoá nitrogen trong tự nhiên,... |
|---|
Bài 1: Trong lò luyện gang, xảy ra phản ứng oxi hóa – khử theo sơ đồ:
Fe2O3+ CO \(\xrightarrow{{{t^o}C}}\) Fe + CO2
Về bản chất, phản ứng oxi hóa - khử là gì, dựa vào dấu hiệu nào để nhận ra loại phản ứng đó?
Làm thế nào để lập phương trình hóa học của phản ứng trên.
Hướng dẫn giải
- Về bản chất, phản ứng oxi hóa – khử là phản ứng xảy ra đồng thời quá trình nhường và quá trình nhận electron.
- Dấu hiệu để nhận ra loại phản ứng oxi hóa – khử là có sự thay đổi số oxi của các nguyên tử.
- Các bước lập phương trình hóa học của phản ứng oxi hóa – khử:
Bước 1: Xác định các nguyên tử có sự thay đổi số oxi hóa, từ đó xác định chất oxi hóa, chất khử
Nguyên tử Fe và C có sự thay đổi số oxi hóa, Fe là chất oxi hóa, C là chất khử
Bước 2: Biểu diễn quá trình oxi hóa, quá trình khử
Fe+3 + 3e → Fe0
C+2 → C+4 + 2e
Bước 3: Tìm hệ số thích hợp cho chất khử và chất oxi hóa dựa trên nguyên tắc tổng electron nhường bằng tổng electron nhận.
2x /Fe+3 + 3e → Fe0
3x /C+2 → C+4 + 2e
Bước 4: Đặt hệ số của chất oxi hóa và chất khử vào sơ đồ phản ứng.
Fe2O3+ 3CO \(\xrightarrow{{{t^o}C}}\) 2Fe + 3CO2
Bài 2: Phản ứng giữa HNO3 với FeO tạo khí NO. Tổng hệ số các chất sản phẩm trong phương trình hóa học của phản ứng này (số nguyên, tối giản) là
A. 8
B. 9
C. 12
D. 13
Hướng dẫn giải
Đáp án: B
3FeO + 10(NO3)3 + NO + 5H2O
Tổng hệ số các chất sản phẩm là 3 + 1 + 5 = 9
Sau bài học này, học sinh có thể:
- Nêu được khái niệm và xác định được số oxi hoá của nguyên tử các nguyên tố trong hợp chất.
- Nêu được khái niệm và ý nghĩa của phản ứng oxi hoá - khử.
- Lập được phương trình hoá học của phản ứng oxi hoá - khử bằng phương pháp thăng bằng electron
- Mô tả được một số phản ứng oxi hoá - khử quan trọng trong cuộc sống.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 10 Kết nối tri thức Bài 15 cực hay có đáp án và lời giải chi tiết.
Một dung dịch chứa 0,01 mol Mg2+, 0,03 mol Na+, x mol Cl- và y mol PO43−. Tổng khối lượng các muối tan có trong dung dịch là 2,59 gam. Giá trị của x và y lần lượt là:
X + HNO3 → Fe(NO3)3 + NO + H2O. Số chất X thực hiện phản ứng bên dưới?
Cho 9,2 gam Zn và Al vào H2SO4 đặc, nóng thu được 5,6 lít khí SO2 (ở đktc, là sản phẩm khử duy nhất). Tính mAl trong hỗn hợp?
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 10 Kết nối tri thức Bài 15để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Giải câu hỏi 1 trang 73 SGK Hóa học 10 Kết nối tri thức - KNTT
Hoạt động trang 73 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải câu hỏi 2 trang 74 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải câu hỏi 3 trang 75 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải câu hỏi 4 trang 76 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải câu hỏi 5 trang 76 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải câu hỏi 6 trang 76 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải câu hỏi 7 trang 77 SGK Hóa học 10 Kết nối tri thức - KNTT
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Một dung dịch chứa 0,01 mol Mg2+, 0,03 mol Na+, x mol Cl- và y mol PO43−. Tổng khối lượng các muối tan có trong dung dịch là 2,59 gam. Giá trị của x và y lần lượt là:
X + HNO3 → Fe(NO3)3 + NO + H2O. Số chất X thực hiện phản ứng bên dưới?
Cho 9,2 gam Zn và Al vào H2SO4 đặc, nóng thu được 5,6 lít khí SO2 (ở đktc, là sản phẩm khử duy nhất). Tính mAl trong hỗn hợp?
Hoà tan mấy gam Al trong HNO3 loãng thấy thoát ra 44,8 lít hỗn hợp 3 khí NO, N2O và N2 có tỉ lệ mol tương ứng là 1:2:2.
Cho FeS2 + HNO3 → Fe(NO3)3 + H2SO4 + NO + H2O, tổng hệ số cân bằng là gì?
Phản ứng oxi hóa – khử lần lượt là?
a) SO3 + H2O → H2SO4
b) CaCO3 + 2HCl → CaCl2 + CO2 + H2O
c) C + H2O → CO + H2
d) CO2 + Ca(OH)2 → CaCO3 + H2O
e) Ca + 2H2O → Ca(OH)2 + H2
f) 2KMnO4 → K2MnO4 + MnO2 + O2
Hệ số chất bị khử trong C6H5C2H5 + KMnO4 → C6H5COOK + MnO2 + K2CO3 + KOH + H2O là mấy?
Cho 0,15 mol oxit sắt nào sau đây tác dụng với HNO3 đun nóng để thu được 0,05 mol NO.
Tổng hệ số của chất khử và oxi hóa FeSO4 + K2Cr2O7 + H2SO4 → Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O?
Tính khử HCl ở phản ứng:
(a) 4HCl + PbO2 → PbCl2 + Cl2 + 2H2O.
(b) HCl + NH4HCO3 → NH4Cl + CO2 + H2O.
(c) 2HCl + 2HNO3 → 2NO2 + Cl2 + 2H2O.
(d) 2HCl + Zn → ZnCl2 + H2.
Xác định số oxi hóa của nguyên tử Fe và S trong các chất sau:
a) Fe, FeO, Fe2O3, Fe(OH)3, Fe3O4.
b) S, H2S, SO2, SO3, H2SO4, Na2SO3.
Xác định chất oxi hóa, chất khử
Chuẩn bị: đinh sắt, dung dịch CuSO4, dung dịch H2SO4 loãng, ống nghiệm.
Thực hiện:
Thí nghiệm 1: Cho đinh sắt vào ống nghiệm đựng dung dịch CuSO4.
Thí nghiệm 2: Cho đinh sắt vào ống nghiệm đựng dung dịch H2SO4.
Quan sát hiện tượng và trả lời câu hỏi:
1. Viết quá trình oxi hóa, quá trình khử.
2. Xác định chất oxi hóa, chất khử trong hai phản ứng trên.
Trong không khí ẩm, Fe(OH)2 màu trắng xanh chuyển dần sang Fe(OH)2 màu trắng xanh chuyển dần sang Fe(OH)3 màu nâu đỏ:
Fe(OH)2 + O2 + H2O → Fe(OH)3
a) Hãy xác định các nguyên tử có sự thay đổi số oxi hóa.
b) Viết quá trình oxi hóa, quá trình khử.
c) Dùng mũi tên biểu diễn sự chuyển electron từ chất khử sang chất oxi hóa
Xét các phản ứng hóa học xảy ra trong công nghiệp:
a) N2 + H2 → NH3
b) Al(OH)3 → Al2O3 + H2O
c) C+CO2 → CO
Phản ứng nào là phản ứng oxi hóa – khử? Lập phương trình hóa học của phản ứng oxi hóa – khử theo phương pháp thăng bằng electron.
Nêu một số phản ứng oxi hóa – khử có lợi và có hại trong thực tế.
Lập phương trình hóa học của các phản ứng trong quá trình sản xuất sulfuric acid theo sơ đồ mục IV.3. Trong các phản ứng đó, phản ứng nào là phản ứng oxi hóa – khử?
Đèn xì ogygen – acetylene có cấu tạo gồm hai ống dẫn khí: một ống dẫn khí oxygen, một ống dẫn khí acetylene (Hình 15.1). Khi đèn hoạt động, hai khí này được trộn vào nhau để thực hiện phản ứng đốt cháy theo sơ đồ:
C2H2 + O2 → CO2 + H2O
Phản ứng tỏa nhiệt lớn, tạo ra ngọn lửa có nhiệt độ đạt đến 30000C nên được dùng để hàn cắt kim loại.
Hãy xác định chất oxi hóa, chất khử và lập phương trình hóa học của phản ứng trên theo phương pháp thăng bằng electron.
Trong quá trình luyện gang từ quặng chứa Fe2O3, ban đầu không khí nóng được nén vào lò cao, đốt cháy hoàn toàn than cốc kèm theo tỏa nhiệt mạnh:
C + O2 → CO2
Khí CO2 đi lên phía trên, gặp các lớp than cốc và bị khử thành CO:
CO2 + C → CO
Tiếp đó, khí CO khử Fe2O3 theo phản ứng tổng quát:
Fe2O3 + CO → Fe + CO2
Lập các phương trình hóa học ở trên, chỉ rõ chất oxi hóa, chất khử
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *