Mời các em học sinh cùng tham khảo nội dung bài học Bài 10: Quy tắc Octet môn Hóa 10 chương trình SGK Kết nối tri thức được đội ngũ DapAnHay biên soạn và tổng hợp bên dưới đây để nắm được cách vận dụng quy tắc octet trong quá trình hình thành liên kết hoá học cho các nguyên tố nhóm A cùng như giải thành thạo một số bài toán liên quan.
- Theo thuyết cấu tạo hoá học, sự liên kết giữa các nguyên tử tạo thành phân tử hay tinh thể được giải thích bằng sự giảm năng lượng khi các nguyên tử kết hợp lại với nhau. Khi tạo liên kết hoá học thì nguyên tử có xu hướng đạt tới cấu hình electron bền vững của khí hiếm.
- Liên kết hoá học là sự kết hợp giữa các nguyên tử tạo thành phân tử hay tinh thể bền vững hơn.
- Trong các phản ứng hoá học, chỉ có các electron thuộc lớp ngoài cùng và phân lớp sát lớp ngoài cùng tham gia vào quá trình tạo thành liên kết (electron hoá trị).
- Các electron hoá trị của nguyên tử một nguyên tố được quy ước biểu diễn bằng các dấu chấm đặt xung quanh kí hiệu nguyên tố.
Bảng 10.1. Biểu diễn electron hoá trị của một số nguyên tử
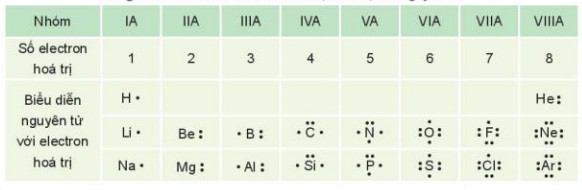
| Liên kết hoá học là sự kết hợp giữa các nguyên tử tạo thành phân tử hay tinh thể bền vững hơn. |
|---|
- Khi hình thành liên kết hoá học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững của nguyên tử khí hiếm. Vì các khí hiếm (trừ helium) đều có 8 electron lớp ngoài cùng nên quy tắc này được gọi là quy tắc octet.
- Khi hình thành liên kết hoá học trong phân tử Cl2, nguyên tử chlorine có 7 electron hoá trị, mỗi nguyên tử chlorine cần thêm 1 electron để đạt cấu hình electron bão hoà theo quy tắc octet nên mỗi nguyên tử chlorine góp chung 1 electron.
- Phân tử Cl2 được biểu diễn 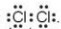
- Xung quanh mỗi nguyên tử chlorine đều có 8 electron.
- Khi hình thành liên kết hoá học trong phân tử H2O, nguyên tử hydrogen có 1 electron hoá trị, nguyên tử oxygen có 6 electron hoá trị, mỗi nguyên tử hydrogen cần thêm 1 electron và nguyên tử oxygen cần thêm 2 electron để đạt cấu hình electron bão hoà theo quy tắc octet.
- Phân tử H2O được biểu diễn 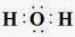 . Xung quanh nguyên tử oxygen có 8 electron.
. Xung quanh nguyên tử oxygen có 8 electron.
- Khi hình thành liên kết hoá học trong phân tử NaF, nguyên tử Na có 1 electron hoá trị, nguyên tử F có 7 electron hoá trị, nguyên tử Na nhường 1 electron hoá trị tạo thành hạt mang điện tích dương, nguyên tử F nhận 1 electron tạo thành hạt mang điện tích âm. Các hạt này đều đạt cấu hình electron bão hoà theo quy tắc octet và có điện tích trái dấu nên hút nhau.
- Quy tắc octet chỉ đúng cho sự tạo thành liên kết hoá học giữa các nguyên tử của các nguyên tố thuộc chu kì 2 của bảng tuần hoàn và một số nguyên tử của các nguyên tố có tính kim loại, phi kim điển hình. Ngoài ra có các ngoại lệ.
Ví dụ: Trong phân tử PCl5, lớp ngoài cùng của P có 10 electron.

| Quy tắc octet: Khi hình thành liên kết hoá học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững của nguyên tử khí hiếm. |
|---|
Bài 1: Khi các nguyên tử kết hợp với nhau tạo thành phân tử theo một tỉ lệ xác định, yếu tố nào quyết định tỉ lệ số nguyên tử của mỗi nguyên tố trong phân tử đó?
Hướng dẫn giải
Hầu hết nguyên tử các nguyên tố trong bảng tuần hoàn đều không đủ 8 electron lớp ngoài cùng nên có xu hướng đạt cấu hình electron bền vững bằng cách kết hợp với các nguyên tử khác theo tỉ lệ nhất định.
Bài 2: Trình bày sự hình thành ion lithium. Cho biết ion lithium có cấu hình electron của khí hiếm tương ứng nào?
Hướng dẫn giải
- Nguyên tử Lithium cho đi 1 electron để tạo thành ion lithium
- Ion lithium có cấu hình electron của khí hiếm He
Bài 3: Vận dụng quy tắc octet, trình bày sơ đồ mô tả sự hình thành phân tử potassium chloride (KCI) từ nguyên tử của các nguyên tố potassium và chlorine
Hướng dẫn giải
- Phân tử potassium được hình thành bởi các ion K+ và Cl-.
- Nguyên tử nguyên tố potassium cho đi 1 electron tạo thành K+ để đạt cấu hình electron bền vững của Ar
- Nguyên tử nguyên tố chloride nhận 1 electron tạo thành Cl- để đạt cấu hình electron bền vững của Ar
Sau bài học này, học sinh có thể:
- Trình bày và vận dụng được quy tắc octet trong quá trình hình thành liên kết hoá học cho các nguyên tố nhóm A.
Các em có thể hệ thống lại nội dung kiến thức đã học được thông qua bài kiểm tra Trắc nghiệm Hóa học 10 Kết nối tri thức Bài 10 cực hay có đáp án và lời giải chi tiết.
Theo quy tắc octet: Trong quá trình hình thành liên kết hóa học, nguyên tử các nguyên tố nhóm A có xu hướng tạo thành lớp vỏ ngoài cùng có
Liên kết hoá học là
Theo quy tắc octet, khi hình thành liên kết hoá học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững giống như
Câu 4-10: Mời các em đăng nhập xem tiếp nội dung và thi thử Online để củng cố kiến thức về bài học này nhé!
Các em có thể xem thêm phần hướng dẫn Giải bài tập Hóa học 10 Kết nối tri thức Bài 10để giúp các em nắm vững bài học và các phương pháp giải bài tập.
Giải câu hỏi 1 trang 49 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải câu hỏi 2 trang 49 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải câu hỏi 3 trang 50 SGK Hóa học 10 Kết nối tri thức - KNTT
Giải câu hỏi 4 trang 50 SGK Hóa học 10 Kết nối tri thức - KNTT
Trong quá trình học tập nếu có thắc mắc hay cần trợ giúp gì thì các em hãy comment ở mục Hỏi đáp, Cộng đồng Hóa học DapAnHay sẽ hỗ trợ cho các em một cách nhanh chóng!
Chúc các em học tập tốt và luôn đạt thành tích cao trong học tập!
Theo quy tắc octet: Trong quá trình hình thành liên kết hóa học, nguyên tử các nguyên tố nhóm A có xu hướng tạo thành lớp vỏ ngoài cùng có
Liên kết hoá học là
Theo quy tắc octet, khi hình thành liên kết hoá học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt tới cấu hình electron bền vững giống như
Khi hình thành liên kết hoá học, nguyên tử có số hiệu nào sau đây có xu hướng nhường 2 electron để đạt cấu hình electron bền vững theo quy tắc octet?
Nguyên tử nguyên tố nào sau đây có xu hướng đạt cấu hình electron bền vững của khí hiếm argon khi tham gia hình thành liên kết hóa học?
Trog công thức CS2, tổng số cặp electron lớp ngoài cùng của C và S chưa tham gia liên kết là
Nguyên tử có cấu hình electron bền vững là
Để đạt quy tắc octet, nguyên tử của nguyên tố potassium (Z = 19) phải nhường đi
Công thức cấu tạo nào sau đây không đủ electron theo quy tắt octet?
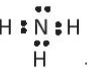
.JPG)
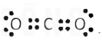

Các nguyên tử kết hợp lại với nhau nhằm mục đích tạo thành cấu trúc mới
Khi nguyên tử fluorine nhận thêm 1 electron thì ion tạo thành có cấu hình electron của nguyên tử nguyên tố nào?
Để giảm năng lượng, các nguyên tử kết hợp lại thành phân tử theo xu hướng nào?
Vận dụng quy tắc octet để giải thích sự hình thành liên kết trong các phân tử F2, CCl4 và NF3.
Phosphine là hợp chất hoá học giữa phosphorus với hydrogen, có công thức hoá học là PH3. Đây là chất khí không màu, có mùi tỏi, rất độc, không bền, tự cháy trong không khí ở nhiệt độ thường và tạo thành khối phát sáng bay lơ lửng. Phosphine sinh ra khi phân huỷ xác động, thực vật và thường xuất hiện trong thời tiết mưa phùn (hiện tượng “ma trơi"). Vận dụng quy tắc octet để giải thích sự tạo thành liên kết hoá học trong phosphine.
Họ và tên
Tiêu đề câu hỏi
Nội dung câu hỏi

0 Bình luận
Để lại bình luận
Địa chỉ email của hạn sẽ không được công bố. Các trường bắt buộc được đánh dấu *